
- 收藏
- 加入书签
线性B细胞表位预测方法的生物信息学研究现状与前沿进展
摘要:在生物技术与生物信息学及人工智能交叉融合的下,免疫研究领域正迎来前所未有的发展机遇。线性 B 细胞表位作为抗原分子中引发特异性免疫应答的关键片段,其精准预测对疫苗研发、疾病早期诊断及靶向免疫治疗的创新具有不可替代的作用。本文系统阐述了线性 B 细胞表位预测的核心理论基础与技术路径,涵盖基于氨基酸序列特征、分子结构解析及智能算法建模等多元预测方法,详细介绍了当前主流的生物信息学数据库与工具的核心功能及应用场景,深入剖析了各类技术的优势与现存局限,并对该领域未来的发展方向进行了展望,旨在突破线性B 细胞表位预测技术的升级与产业化应用。
关键词:线性B 细胞表位;生物信息学;预测工具;序列分析;免疫应答
1 引言
1.1 线性 B 细胞表位的定义与生物学意义
抗原表位(epitope),又称抗原决定簇,是抗原分子中被免疫系统精准识别并启动免疫应答的特定功能区域[1],按识别主体分为B 细胞表位与 T 细胞表位[2]。B 细胞表位可与 B 细胞抗原受体(BCR)或相关抗体特异性结合,依空间结构分为线性表位与构象性表位[3]。线性B 细胞表位由 6-8 个连续氨基酸残基构成[4],与抗体结合不依赖抗原空间折叠,仅通过线性序列实现特异性作用[5]。这一特性使其成为免疫研究核心靶点,为疫苗设计、抗体药物研发等奠定基础。
1.2 研究背景与技术需求
尽管 90% 的天然B 细胞表位为构象性,但多数含连续残基核心区域[6]。与构象性表位相比,线性表位预测无需模拟动态空间构象[7],在生物计算预测中更具优势。线性表位在生物技术和临床应用中备受关注[8],如疾病诊断[9]、疫苗和治疗性抗体的开发[10]。精准定位线性表位能够为多肽疫苗、重组疫苗的设计提供明确靶点[11],大幅缩短研发周期。在疾病诊断领域,基于线性表位的检测技术可显著提升诊断的特异性与灵敏度[12]。然而,传统的线性B细胞表位鉴定依赖于体外多肽合成、ELISA 检测等实验手段,存在流程繁琐、耗时费力、成本高昂等问题,难以满足大规模、高通量的研究需求。所以,计算机模拟预测方法通过预测表位区域[13],可以显著减轻识别工作量,因此它们在此类任务中变得至关重要[14]。
1.3 研究目的与应用价值
开发高可靠性人工智能预测工具,可提升预测精准度、缩短研究周期、降低筛选成本,同时揭示表位与抗体结合规律,为理解免疫识别机制提供支撑。不仅推动免疫应答调控、抗原-抗体相互作用等基础研究,更能加速新型疫苗与治疗性抗体药物的研发进程,为疾病防控提供技术保障。
2 线性B 细胞表位预测的理论基础与技术方法
2.1 预测原理的核心逻辑
线性 B 细胞表位的预测原理源于对其生物学特性与分子相互作用规律的深入解析[15]。早期预测依赖X 射线晶体衍射、核磁共振等结构生物学技术解析抗原-抗体复合物三维结构以确定线性表位,但其操作复杂、成本高,难以推广。
随着生物信息学的发展,预测原理逐渐转向多维度特征整合:一方面,通过分析亲水性[16]、柔韧性[17]、转向[18]和溶剂可及性[19]等氨基酸序列理化性质筛选潜在表位(如亲水性残基易暴露并结合抗体);另一方面结合抗原二级结构特征(高柔韧性区域更易与抗体互补结合),同时整合序列、结构等多维度特征构建泛化模型,实现线性 B 细胞表位的高效精准预测。
2.2 主流预测技术方法解析
2.2.1 基于氨基酸序列特征的预测方法
该方法是线性B 细胞表位预测的经典范例,通过分析氨基酸序列的理化性质与序列模式筛选潜在表位区域。其中主要通过Hopp-Woods、Kyte-Doolittle 等量表量化亲水性,通过残基旋转自由度评估柔韧性,结合序列保守性、免疫原性等特征设定阈值,筛选潜在表位。
优势:计算逻辑简单、运算速度快,无需复杂的计算资源与结构数据支持,适用于大规模序列的初步筛选,可快速缩小候选表位范围。
局限性:仅依赖单一维度的序列特征,忽略了氨基酸残基间的相互作用及序列所处的局部环境影响,预测准确性有限,需要与其他方法结合使用。
2.2.2 基于分子结构特征的预测方法
以抗原分子的三维结构为核心,通过表面电荷分布、氢键形成潜力、疏水作用等分析预测抗原表位。
优势:从空间结构层面揭示结合机制,预测准确性高于序列特征分析,可为表位的功能验证提供更可靠的候选靶点。
局限性:依赖高质量的抗原分子三维结构数据,计算资源需求高,对缺乏结构信息的抗原适用性差。
2.2.3 基于机器学习算法的预测方法
随着机器学习技术的进步,基于大量蛋白质序列和结构数据集训练的模型[20],现已能够仅凭氨基酸序列准确预测局部和全局蛋白质结构特征[21],这类方法通过构建数学模型,从大量标注数据中学习表位与非表位序列的特征差异,实现精准分类预测。
(1)支持向量机(SVM):作为常用算法,通过构建最优超平面实现表位与非表位序列的二分类[22]。在应用过程中,需先将氨基酸序列转化为特征向量,再通过选择合适的核函数映射到高维空间,解决非线性分类问题。优势:泛化能力强,对高维数据的处理效果优异;局限性:对特征选择与参数优化的依赖性强,参数设置不当易导致模型过拟合或欠拟合,影响预测准确性。
(2)人工神经网络(ANN):模拟生物神经系统的信息处理模式[23],构建由输入层、隐藏层和输出层组成的网络模型,能自动学习序列中的复杂特征与潜在关联。优势:对非线性关系的拟合能力强,无需人工干预特征工程,可自动提取高阶特征;局限性:需要大量标注数据进行模型训练,计算成本高、训练周期长,且模型解释性较差。
(3)随机森林(RF):基于集成学习思想,通过构建多个决策树并综合其预测结果提升模型的稳定性与准确性。优势:可同时整合氨基酸序列的理化性质、结构特征、序列模式等多维度信息,抗噪声能力强,能有效避免过拟合,对高维数据的处理效果良好;局限性:预测性能受决策树数量、树深度等参数影响较大,在处理极度不平衡的数据集时,预测结果可能偏向多数类样本。
(4)递归神经网络(RNN):专门处理序列数据的深度学习算法,能够捕捉氨基酸序列中的时序依赖关系,适用于分析线性 B 细胞表位的序列连续性特征[24]。优势:适配线性表位的序列连续性特征,可有效捕捉长序列中的关键信息;局限性:训练数据需求量大,计算成本高,模型优化难度较大
表 1 主流线性B 细胞表位预测方法对比

3 核心生物信息学资源与工具
3.1 关键数据库资源
高质量的数据库是线性 B 细胞表位预测模型构建、方法验证及应用研究的基础。目前,全球已建立多个综合性或专业性免疫表位数据库,提供了丰富的数据支撑。
(1)免疫表位数据库(Immune Epitope Database, IEDB)是目前全球最全面的综合性免疫表位数据库[25],由美国国立卫生研究院(NIH)支持建立,涵盖B 细胞表位、T 细胞表位等多种免疫相关数据,整合文献报道、实验验证及临床研究的海量数据,为每个线性 B 细胞表位提供氨基酸序列、来源抗原等详细信息,支持多条件检索与数据下载,集成多种在线预测工具,是该领域核心资源。
(2)B 细胞表位数据库(BCEepitope)专注于 B 细胞表位的专业数据库,重点收录经实验验证的线性B 细胞表位数据,详细标注抗原来源、抗体结合亲和力等功能信息,提供抗原分子三维结构链接,支持按抗原类型、物种等分类检索,适用于疫苗研发与抗体药物开发相关的表位筛选。
(3)抗原表位数据库(EpitomeDB)注重于抗原表位数据整合与共享的数据库,收录了来自不同物种、不同疾病相关的线性 B 细胞表位数据[26],整合序列、结构、免疫应答等多维度信息,数据标准化程度高、审核严格,提供序列比对与进化分析功能,为通用型疫苗设计提供支持。
表 2 主流免疫表位数据库对比

3.2 主流预测工具
随着预测技术的发展,一系列高效的在线预测工具与离线软件被开发并应用,为线性 B细胞表位预测提供了便捷的技术支持。
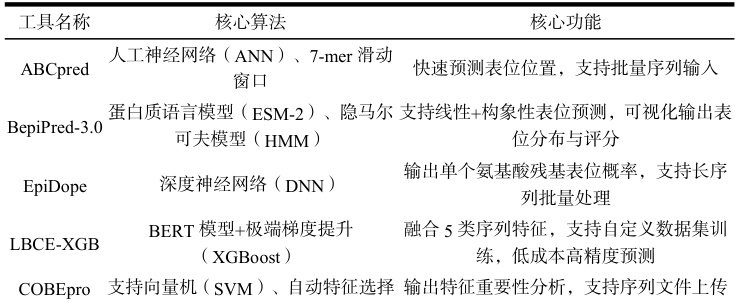
(1)ABCPred:是一款广泛应用的线性B 细胞表位预测工具[27],基于人工神经网络算法构建,核心通过分析抗原分子的氨基酸序列预测潜在表位区段[28]。采用7-mer 滑动窗口策略,将氨基酸序列转化为基于理化性质的特征向量,输入神经网络模型进行训练与预测。核心优势:操作简便,仅需输入抗原的氨基酸序列,即可快速获得预测结果(含表位位置、置信度得分),支持批量输入序列进行预测,适用于大规模抗原的表位筛选,在病毒疫苗研发、抗体药物设计等领域得到了广泛应用。
(2)BepiPred-3.0::目前应用最广泛的线性B 细胞表位预测工具之一[29],经过多轮版本迭代后,已从早期的单一特征整合升级为基于蛋白质语言模型的预测工具[30]。该工具利用蛋白质语言模型 ESM-2 的数值表示[31],结合隐马尔可夫模型(HMM)进行预测,用户只需上传 fasta 格式的蛋白质序列[32],即可获得可视化的预测结果,包括表位区域分布与置信度评分,适用于各类抗原的表位筛选研究。
(3)EpiDope 是一款基于深度神经网络(DNN)的线性 B 细胞表位预测工具[33],利用深度神经网络检测单个蛋白质序列上线性B 细胞表位区域的 Python 工具[34]。核心创新:通过深度神经网络模型自动学习抗原序列与表位活性之间的复杂关联,无需人工设计特征,能够捕捉氨基酸序列中的高阶模式。优势:预测准确性高,尤其适用于长序列抗原的表位筛选,支持批量处理数据,输出结果包含每个氨基酸残基的表位概率得分,方便精确定位核心表位区域,在细菌抗原、肿瘤抗原等表位预测中表现出色。
(4)LBCE-XGB:融合机器学习与深度学习技术的新型预测工具[35],核心整合了极端梯度提升(XGBoost)算法与自然语言处理中的BERT 模型[36]。工作流程分为两步:首先通过预训练的表位专一性 BERT 模型提取多肽序列中的深层生物学信息,生成残基嵌入向量;随后结合氨基酸组成、抗原性量表、理化性质、二级结构特征等五种序列特征,共同输入 XGBoost算法进行模型训练。LBCE-XGB 在性能测试中表现优异,显著优于同类工具。优势:以低成本实现了高精度预测,同时支持自定义数据集训练,适用于针对特定病原体或抗原的表位预测研究,为个性化疫苗研发提供了有力支持[37]。
(5)COBEpro 是基于支持向量机的线性B 细胞表位预测工具,整合氨基酸理化性质、序列模式及结构特征开展预测。其特色为独特特征选择策略,可自动筛选高贡献特征,提升模型预测准确性与泛化能力。工具支持输入抗原氨基酸序列或上传文件,输出表位区域、置信度得分及特征重要性分析,在病原体表位预测中表现良好,尤其适用于新型病原体的快速表位筛选。
表 3 主流线性 B 细胞表位预测工具对比
4 总结与展望
尽管线性 B 细胞表位预测技术已取得显著进展,但仍面临诸多需要解决的问题[38]。预测准确性有待进一步提升,不同工具的预测模型、特征选择与数据集存在差异,导致难以客观比较其性能优劣,随着生物信息学技术、人工智能算法与多组学研究的不断融合,线性 B细胞表位预测领域有望迎来突破性发展[39]。
算法创新将持续推动预测性能提升,未来将有更多新型深度学习框架应用于表位预测,通过更高效的特征提取与模型构建,进一步提高预测的准确性与稳定性。能够为表位预测提供更全面的生物学信息,实现从“序列层面”到“功能层面”的精准预测,尤其适用于新型病原体与肿瘤抗原的表位筛选。
线性B 细胞表位预测技术作为免疫研究与生物技术转化的核心支撑,尽管当前技术仍面临预测准确性、数据标准化等方面的挑战,但随着生物信息学、人工智能算法与多组学研究的深度融合,线性B 细胞表位预测技术将不断迭代升级。未来,通过算法创新、数据整合、平台建设与临床转化的协同发展,该技术有望为免疫学基础研究提供新的理论视角,为疾病防控与精准治疗提供更强大的技术保障,应用前景广阔。
参考文献:
[1]Pishesha N, Harmand T J, Ploegh H L. A guide to antigen processing and presentation[J]. Nature Reviews Immunology, 2022, 22(12): 751-764.
[2]Bukhari S N H, Jain A, Haq E, et al. Machine learning techniques for the prediction of B-cell and T-cell epitopes as potential vaccine targets with a specific focus on SARS-CoV-2 pathogen: a review[J]. Pathogens, 2022, 11(2): 146.
[3]张佳琦, 王亚玉, 郭兴, 等. 基于单个 B 淋巴细胞扩增技术筛选马传染性贫血病毒的 囊膜蛋白单克隆抗体[J]. Chinese Journal of Preventive Veterinary Medicine/Zhongguo Yufang Shouyi Xuebao, 2022, 44(3).
[4]Kumar N, Tripathi S, Sharma N, et al. A method for predicting linear and conformational B-cell epitopes in an antigen from its primary sequence[J]. Computers in Biology and Medicine, 2024, 170: 108083.
[5]吕红强, 郝乐乐, 刘二虎, 等. 基于生物信息学的 Hi-C 研究现状与发展趋势[J]. 遗传, 2019, 42(1): 87-99.
[6]Kringelum JV, Nielsen M, Padkjær SB, Lund O. Structural analysis of b-cell epitopes in antibody: Protein complexes. Mol Immunol. 2013; 53(1–2): 24–34.
[7]Cia G, Pucci F, Rooman M. Critical review of conformational B-cell epitope prediction methods[J]. Briefings in bioinformatics, 2023, 24(1): bbac567.
[8]Behmard E, Soleymani B, Najafi A, Barzegari E. Immunoinformatic design of a covid-19 subunit vaccine using entire structural immunogenic epitopes of sars-cov-2. Sci Rep. 2020; 10(1): 20864.
[9]Mucci JJ, Carmona S, Volcovich R, Altcheh J, Bracamonte ED, Marco J, Nielsen MA, Buscaglia C, Agüero F. Next-generation ELISA diagnostic assay for chagas disease based on the combination of short peptidic epitopes. PLOS Negl Trop Dis. 2017;11(10):e0005972.
[10]Kozlova EEG, Cerf L, Schneider FS, et al. Computational b-cell epitope identification and production of neutralizing murine antibodies against atroxlysin-i. Sci Rep. 2018; 8(1): 14904.
[11]石刚, 邓洪新. 肿瘤治疗性疫苗的研发现状与展望[J]. Chinese Journal of Cancer Biotherapy, 2023, 30(7).
[12]闻丹忆. 体外诊断的开发前沿与应用进展[J]. 药学进展, 2023, 47(6): 401-403.
[13]Sanchez-Trincado JL, Gomez-Perosanz M, Reche PA. Fundamentals and methods for t- and b-cell epitope prediction. J Immunol Res. 2017; 2017: 2680160.
[14]Shirai H, Prades C, Vita R, et al. Antibody informatics for drug discovery. Biochem Biophys Acta Proteins Proteomics. 2014; 1844(11): 2002–2015.
[15]张林涵, 陈建华. 免疫信息学预测在治疗蛋白研究中的应用与发展[J]. Pharmacy Information, 2023, 12: 184.
[16]Parker JM, Guo D, Hodges RS. New hydrophilicity scale derived from high-performance liquid chromatography peptide retention data: correlation of predicted surface residues with antigenicity and X-ray-derived accessible sites. Biochemistry. 1986;25:5425–32.
[17]Karplus PA, Schulz GE. Prediction of chain flexibility in proteins - a tool for the selection of peptide antigens. Nature (London). 1985;72:212–3.
[18]Chou PY, Fasman GD. Prediction of the secondary structure of proteins from their amino acid sequence. Adv Enzymol Relat Areas Mol Biol. 1978;47:45–148.
[19]Emini EA, Hughes JV, Perlow DS, Boger J. Induction of hepatitis A virus-neutralizing antibody by a virus-specific synthetic peptide. J Virol. 1985;55:836–9.
[20]Høie MH, Kiehl EN, Petersen B, et al. NetSurfP-3.0: Accurate and fast prediction of protein structural features by protein language models and deep learning. Nucleic Acids Res. 2022; 50:gkac439.
[21]Jumper J, Evans R, Pritzel A, et al. Highly accurate protein structure prediction with alphafold. Nature. 2021; 596(7873): 583–589.
[22]朱磊, 李光健, 赵兴瑞, 等. 基于双通道分类处理的图像拼接方法[J]. Journal of Xi'an Polytechnic University, 2025, 39(4).
[23]Shao F, Shen Z. How can artificial neural networks approximate the brain?[J]. Frontiers in psychology, 2023, 13: 970214.
[24]左志威, 孟庆良, 崔家康, 等. 基于硬皮病线粒体相关基因的人工神经网络模型的构建[J]. Journal of Southern Medical University, 2024, 44(5): 920.
[25]周婷婷, 冯健男. 抗体信息数据库[J]. Chinese Journal of Biochemistry and Molecular Biology, 2017, 33(8): 750-755.
[26]Liu J, Zhang W. Databases for B-cell epitopes[M]//Immunoinformatics. New York, NY: Springer New York, 2014: 135-148.
[27]Saha S, Raghava GP. Prediction of continuous B-cell epitopes in an antigen using recurrent neural network. Proteins. 2006;65:40–8.
[28]白跃花, 蔡景耀, 林佳. 基于深度学习融合模型的蛋白质–蛋白质互作预测研究[J]. Hans Journal of Biomedicine, 2025, 15: 577.
[29]张林涵, 陈建华. 免疫信息学预测在治疗蛋白研究中的应用与发展[J]. Pharmacy Information, 2023, 12: 184.
[30]Lin Z, Akin H, Rao R, et al. Language models of protein sequences at the scale of evolution enable accurate structure prediction. bioRxiv. 2022.
[31]Rives A, Meier J, Sercu T, et al. Biological structure and function emerge from scaling unsupervised learning to 250 million protein sequences. Proc Natl Acad Sci U S A. 2021; 118(15):e2016239118.
[32]Clifford J N, Høie M H, Deleuran S, et al. BepiPred‐3.0: Improved B‐cell epitope prediction using protein language models[J]. Protein Science, 2022, 31(12): e4497.
[33]谈妍辰, 王文文, 夏结来, 等. 机器学习算法在抗肿瘤药物响应预测中的应用研究[J]. 中国临床药理学与治疗学, 2025, 30(2): 200.
[34]Collatz M、Mock F、Barth E 等人。EpiDope:用于线性B细胞表位预测的深度神经网络[J]。《生物信息学》,2021年,37(4):448-455。
[35]Liu Y, Liu Y, Wang S, et al. LBCE-XGB: a XGBoost model for predicting linear B-Cell epitopes based on BERT embeddings[J]. Interdisciplinary Sciences: Computational Life Sciences, 2023, 15(2): 293-305.
[36]车万翔, 窦志成, 冯岩松, 等. 大模型时代的自然语言处理: 挑战, 机遇与发展[J]. 中国科学: 信息科学, 2023, 53(9): 1645-1687.
[37]Liu Y, Liu Y, Wang S, et al. LBCE-XGB: a XGBoost model for predicting linear B-Cell epitopes based on BERT embeddings[J]. Interdisciplinary Sciences: Computational Life Sciences, 2023, 15(2): 293-305.
[38]欧阳玉梅. 构象性 B 细胞表位预测的免疫信息学方法及其网络资源[J]. Chinese Bulletin of Life Sciences, 2010, 22(9).
[39]刘春宇, 刘子钰, 董娇娇, 等. 线性 B 细胞表位预测的机器学习方法[J]. 计算机光盘软件与应用, 2013, 16(24): 264-265.






 京公网安备 11011302003690号
京公网安备 11011302003690号


