
- 收藏
- 加入书签
基于网络药理学与分子对接探讨异钩藤碱抗动脉粥样硬化的潜在机制
摘要:目的:通过网络药理学及分子对接的方法探讨异钩藤碱治疗动脉粥样硬化的作用机制。方法:使用不同数据库预测最新研究发现的动脉粥样硬化及异钩藤碱作用靶点,获得共同作用靶点。应用 DAVID 数据库进行 GO 及KEGG 分析,并对及分析结果可视化。利用 Auto Dock 软件行分子对接。通过多种途径研究异钩藤碱对于动脉粥样硬化的作用机制。结果:GO 富集分析显示异钩藤碱治疗动脉粥样硬化核心靶点基因主要与细胞对脂多糖的反应、氧化氮生物合成过程等生物学过程有关。KEGG 富集发现其作用机制与脂质和动脉粥样硬化、C 型凝集素受体信号通路相关。分子对接结果示与 TNF、JAK2 等靶点有较好的结合。结论:  所得结果提示异钩藤碱可能通过抗炎、调节脂质代谢等途径发挥抗粥样硬化作用。
所得结果提示异钩藤碱可能通过抗炎、调节脂质代谢等途径发挥抗粥样硬化作用。
关键词:动脉粥样硬化;异钩藤碱;网络药理学;分子对接;
心血管疾病是全球人员死亡的主要原因,每年造成约 1800 万人死亡[1]。造成心血管疾病的原因有多种,动脉粥样硬化(Atherosclerosis,AS)是其中主要原因之一,是血管内斑块形成的过程,包括血管内膜中的各种细胞、脂质和碎片组织[2]。主要累及大中型动脉,特别常见于内皮剪切应力低或血流紊乱的动脉,例如动脉弯曲或分叉部位[3]。现可采取的预防及治疗措施包括危险因素管理、药物干预和外科手术等。目前治疗 AS 的药物干预是临床治疗中最常用的方法,包括降脂药物、抗血小板药物和抗炎药物。而现有常用药物治疗存在各种局限性问题,疾病治疗的有更高的需求,从而新型药物的研发尤为重要。
异钩藤碱(Isorhynchophylline,IRN)为中药钩藤中的吲哚类生物碱,是钩藤主要活性成分[4]。有研究表明,IRN 具有抑制心肌细胞肥大、降压、扩张血管、抗血小板聚集和血栓形成以及神经保护等作用[5-6]。目前已用于临床治疗心血管疾病和中枢神经系统疾病[7]。目前已有动物实验研究发现[8],IRN 可于脂质代谢与稳态维持和高血压的治疗发挥重要作用。本文中利用网络药理学与分子对接的方法研究异钩藤碱对动脉粥样硬化的疾病发展中的作用机制。
材料与方法:
1.1 异钩藤碱与动脉粥样硬化靶点筛选,选取药物、疾病共同靶点
通过利用 SwissTargetPrediction、TCMSP、PharmMapper、CTD、GeneCards 等数据库以“ Isorhynchophylline”为关键词进行检索 IRN 的靶点。于 DrugBank、GeneCards、Therapeutic Target 等数据库以“ Atherosclerosis” 为关键词进行检索 AS 的靶点基因。将得到的结果转换为基因名,下载数据,各自结果汇总至表格数据并去重。将数据库预测的 IRN 与 AS 的靶点导入绘图工具中,绘制共同靶点韦恩图。
.2 蛋白质相互作用(PPI)网络构建及选取核心靶点
于 STRING 数据库导入已获得的共同靶点,以“ Homo sapiens” 为物种,构建蛋白质相互作用网络,将得到的文件导入 Cytoscape 软件进行可视化,绘制共同靶点网络拓扑图。利用阶数中心性(BetweennessCentrality,BC)、筛选度(DegreeCentrality,DC)和中心接近度(Closeness Centrality,CC)等参数排序,取排列于各参数前 15 名的靶点,选取为核心靶点。
1.3 GO 生物过程和 KEGG 信号通路富集分析
将 IRN 与 AS 的核心基因提交到 DAVID Functional Annotation Bioinformatics Microarray Analysis 数据库,选择物种为“ Homo sapiens” 进行 GO 和 KEGG 富集分析,分析后获得 GO 条目为生物过程(Biological process)、细胞组成(Cellular Component)、分子功能(Molecular Function)等。根据富集度(Enrichment score)的数值分别选择前 10 条目,通过微生信网站绘制 GO 分析条形图。于 KEGG 富集分析得到结果,根据P值选择前 20个信号通路,微生信平台绘制气泡图,并绘制靶点-信号通路网络图。
1.4 分子对接
于靶点-信号通路网络和核心靶点中,通过 BC、DC、CC 将选取在各参数中位于前五的靶点。从 RCSB PDB数据库下载靶蛋白 3D 结构。TCMSP 数据库下载 IRN 学结构。利用 PyMOL 软件行去除先分子、脱水等处理,再于分子对接模拟软件 AutoDock,将已脱水分子加氢等处理的靶蛋白进行对接模拟计算。最终记录各个靶蛋白与 IRN 分子结合的结合能及最佳结合位点。
2.结果
2.1 异钩藤碱与动脉粥样硬化靶点筛选,获取药物、疾病共同靶点
在数据库中汇总、去重后获得 IRN 靶点 252 个(图 1),AS 靶点 234 个(图2)。将数据库预测的 IRN 与AS 的所有靶点导入 jvenn 得到共同靶点 27 个,绘制韦恩图(图3)与网络图(图4)。
图 1.IRN 靶点网络图

图 2.AS 网络图

图 3.AS 与 IRN 韦恩图
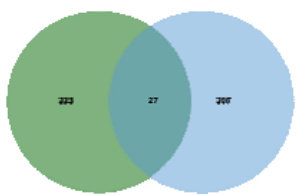
图 4.共同靶点网络图
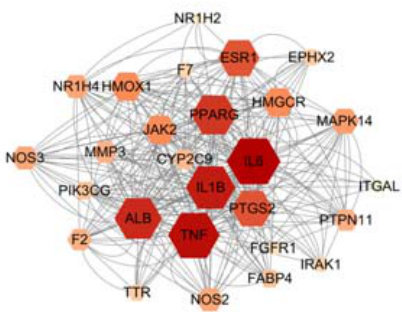
2.2 蛋白质相互作用(PPI)网络构建及选取核心靶点
于 STRING 数据库导入已获得 IRN 与 AS 的共同靶点。利用 BC、DC 和 CC,以 3 个参数排序选取核心靶点得到 17 个。
表1 核心靶点阶数中心性、筛选度、中心接近度值
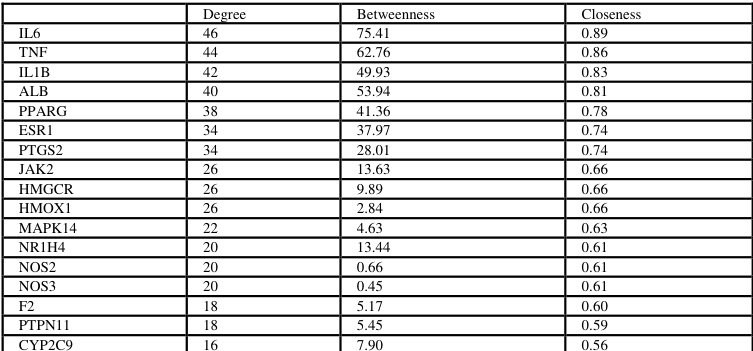
2.3 GO 生物过程和 KEGG 信号通路富集分析
图 5.IRN 与 AS GO 富集分析条形图
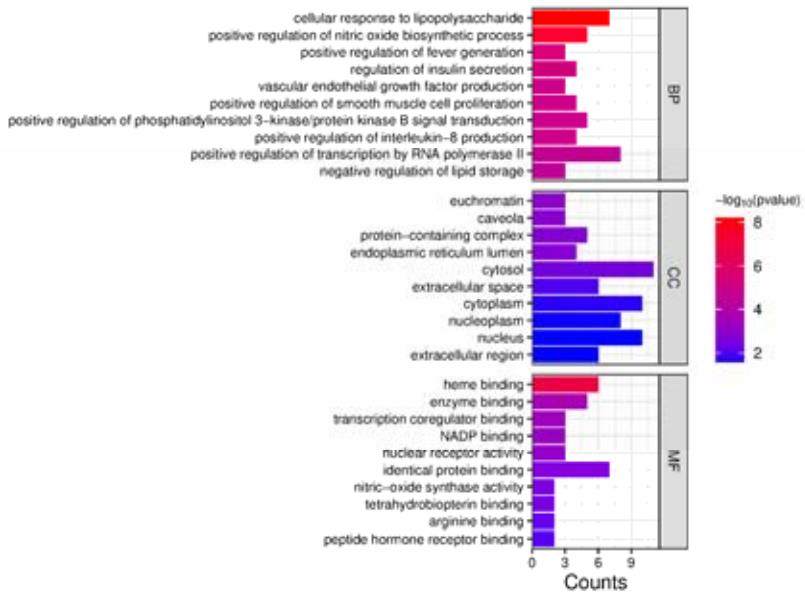
通过 DAVID Functional Annotation Bioinformatics Microarray Analysis 数据库,将核心基因进行 GO 和 KEGG富集分析。获得结果中选取 P 值小于 0.05 的 GO 条目,其中生物过程 57 条目,细胞组成 10 条目,分子功能 20条目。研究表明 P 值越小,可信度越高。生物学过程主要涉及细胞对脂多糖的反应、一氧化氮生物合成过程的调控、血管内皮生长因子的产生等。细胞组分主要涉及常染色质、内质网腔等。分子功能主要涉及血红素结合、酶结合、转录共调节因子结合等,于微生信平台绘制条形图(图 5)。图中表示颜色与 P 值相关,P 值越小,条形图的颜色越红,与治疗 AS 相关性越强,条形图的长度与富集基因数目相关,富集基因越多,条形图的长度越长。KEGG 富集分析后选取 P 值小于 0.05 的得通路 55 条,包括脂质和动脉粥样硬化、C 型凝集素受体信号通路、糖尿病并发症中的 AGE-RAGE 信号通路、IL-17 信号通路等,微生信平台绘制气泡图(图 6)。气泡图圆点由绿色向红色过渡,P 值越小颜色越红,代表通路在治疗 AS 中的作用可能较显著。图中的圆点大小与富集基因数目相关,富集基因越多,气泡图的圆点越大。利用已获得全部通路与其相关靶点绘制靶点-信号通路 PPI 网络图(图 7),通过 BC、DC 和 CC 筛选出各参数位于前五的靶点,结果得到 14 个靶点。
图 6.IRN 与 AS KEGG 富集分析气泡图
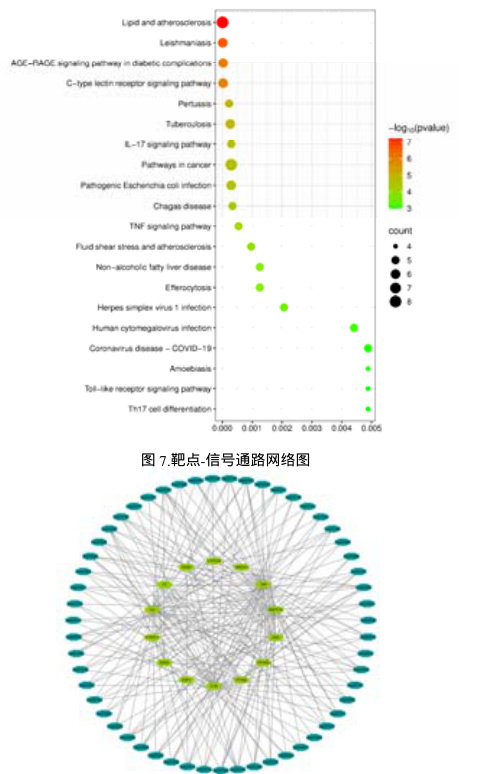
2.4 分子对接
选取靶点-信号通路 PPI 网络中各参数位于前五的靶点与核心靶点中各参数位于前五的靶点,最终筛选出PPARG、TNF、IL6、MAPK14、JAK2 等 5 个靶点。后于分子对接模拟软件 AutoDock 中进行对接模拟计算,得到最佳结合位点及相对结合能。可视化后的 PPARG 与 ASN-429 残基形成氢键;TNF 与 VAL-80、GLU-72、ASP-71残基形成氢键;IL6 与 CYS-481、ASN-484、ASN-479 残基形成氢键;MAPK14 与 ARG-220 残基形成氢键;JAK2与 ILE-973、ASP-976、ASP-994 残基形成氢键。以上氨基酸残基对接结果表示所选择靶点与 IRN 的结合能均大于-3.5kcal/mol,表明与 IRN 的结合能力都较好。
表2.异钩藤碱与潜在靶点对接结果

图 9.分子对接分析结果:编码蛋白 3D 结构与氢键结合图
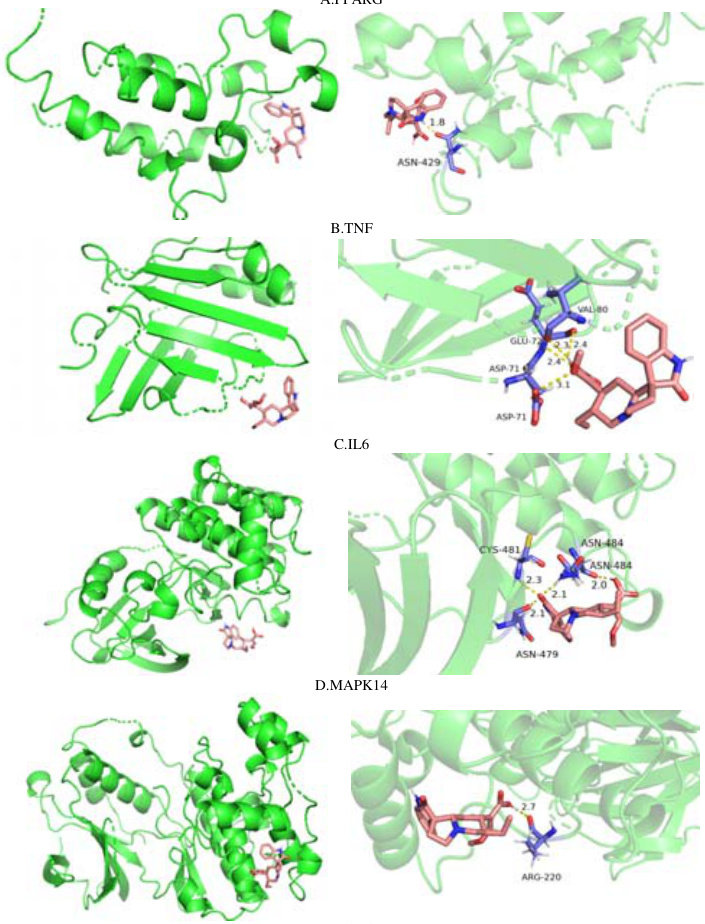
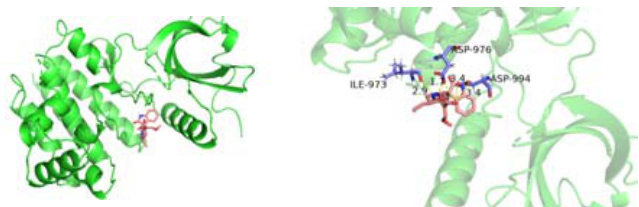
3.讨论
动脉粥样硬化的新药研发近年来进展迅速,从传统的降脂、抗炎治疗扩展到免疫调节、靶向递送等创新领域。不断研究新药,达到精准靶向、长效控制,避免疾病进展及无效治疗。本文中通过网络药理学,网络数据库中查询 IRN 与 AS 的共同作用靶点,再通过 GO 和 KEGG 分析对此靶点进行分析,研究 IRN 治疗 AS 过程中所涉及生物过程及相关信号通路。对所得靶点与 IRN 通过分子对接,评估蛋白与药物分子之间结合是否稳定。最终了解治疗 AS 的作用机制,得到 IRN 通过多种靶点,以多种途径达到我们预想的治疗成果。
GO 分析结果表明 IRN 作用于细胞对脂多糖的反应、一氧化氮生物合成过程的调控、调节胰岛素分泌、血管内皮生长因子的产生等生物工程。AS 的发生与内皮细胞损伤、脂质沉积、炎症反应、平滑肌细胞增殖迁移等相关。脂多糖(LPS)引起脂质代谢紊乱,在 AS 的发展中起重要作用,可以促进它的发展[9]。LPS 通过调节 NF-κ B 和 MAPK 通路促进各种炎症因子的产生和释放,从而发生炎症反应[10]。生理性低浓度的一氧化氮维持血管稳态,主要通过扩散到周围细胞中并与可溶性鸟苷酸环化酶结合。这导致第二信使环状鸟苷酸单磷酸盐(cGMP)的细胞浓度增加,进而激活蛋白激酶 G(PKG)。PKG 随后磷酸化 L 型钙通道,导致细胞内钙浓度降低、平滑肌细胞松弛(SMC)与血管舒张[11]。此外,还抑制血管 SMC 增殖和 LDL 氧化,并还可抑制血小板黏附和聚集、白细胞向内皮细胞迁移和黏附。NO 可通过抑制 NF-κ B 活化、抑制黏附分子表达和促进调节性 T 细胞分化达到抗炎作用[12]。胰岛素可通过作用于血管内皮细胞胰岛素受体,激活磷脂酰肌醇-3-激酶(PI3K)信号级联反应,从而增强内皮一氧化氮合酶(eNOS)的活性,形成的 NO 扩散至 SMC 松弛[13]。胰岛素还可通过刺激 PI3K/Akt通路对抗 NO 和对纤溶酶原激活物抑制物、血管细胞黏附分子-1 等多种内皮脉粥样硬化的因子。在胰岛素抵抗条件下,PI3K 通路受损,NO 产生减少,可导致内皮功能障碍。另外,胰岛素抵抗还会刺激血管平滑肌细胞的增殖和脂肪组织中游离脂肪酸的过度释放并参与促动脉粥样硬化脂质分布和血脂异常的发生,因此最终可能参与 AS 的进一步加重[14]。在 AS 斑块中血管内皮生长因子(VEGF)的表达水平显著升高,可增加血管通透,并使血管新生血管壁更为脆弱而薄、内皮细胞间连接不够紧密。因此血管壁易于受损,也使血液中脂质、炎症细胞等更为容易进入其内加重炎症,促进形成 AS 斑块形成[15]。VEGF 也可通过参与 JAK2、Akt、PLC-г 1、Src、FAK 等多种信号通路调节血管内皮细胞的分裂、增殖、迁移及生存 。
KEGG 分析结果显示异钩藤碱通过脂质和动脉粥样硬化、C 型凝集素受体信号通路、IL-17 信号通路、糖尿病并发症中的 AGE-RAGE 信号通路等发挥治疗动脉粥样硬化的。脂质过氧化和 LDL 的氧化会引发动脉粥样硬化的启动和进一步进展,低密度脂蛋白(LDL)受体-1(LOX-1)介导的氧化低密度脂蛋白(ox-LDL)作用于血管内皮细胞,损害其正常抗动脉粥样硬化功能,增强其招募单核细胞的能力,以及诱导泡沫细胞形成[17]。C型凝集素识别受体 2(Dectin-2)在 AS 斑块中表达显著上调,抑制 Dectin-2 表达可以减少 ox-LDL 诱导的 SMC增殖和表型转化。Dectin-2 调控 SMC 的增殖和表型转化过程可能是通过促进了 STAT3 信号活化[18]。JAK/STAT也参与 AS 的发展过程。它通过诱导趋化因子和促炎因子的表达,调控 VSMC 增殖迁移、血管生成等。有研究表明,白细胞介素(IL)-17 可能在动脉粥样硬化和一些致动脉粥样硬化性疾病中发挥作用。IL-17 家族中,IL-17A是最重要的亚型。该细胞因子可能在血管炎发病机制中发挥作用,其特征是血管壁炎症、内皮损伤和组织损伤。IL-17A 在复杂的细胞因子网络中相互作用,促进炎症、血栓形成和凝血。关于这些影响,结果表明这种细胞因子与从动脉粥样硬化到血管炎的各种疾病有关。IL-17A 通过激活组织因子和减少抗凝介质,促进血栓形成和凝血[19-20]。晚期糖基化终末产物(Advanced glycation end products,AGE)是一组通过非酶糖基化作用产生的糖基化终末产物,与晚期糖基化终末产物受体(receptor of advanced glycation end products,RAGE)共同参与糖尿病及其相关并发症的发生发展。有研究发现,糖尿病患者的心血管疾病发展与 AGE-RAGE 信号通路有关。该通路参与内皮损伤,SMC 功能的改变,这些过程共同导致动脉损伤,通过多种机制放大动脉粥样硬化斑块的进展,例如抑制内皮 NO 产生,促进氧化应激、血管内皮细胞中的炎症反应等[21]。
分子对接后表明此次研究的7靶点蛋白与 IRN 分子之间有较高的结合能。分子与靶点已研究得到的结合位点结合时结合能最高,结合可能最佳。通过以上分析得到靶点蛋白与 IRN 分子都有较好的结合能力,其中 TNF结合活性最高。
综上所述,以上研究结果确定异钩藤碱和动脉粥样硬化与 PPARG、TNF、IL6、MAPK14、JAK2 等多种靶点息息相关。IRN 可能参与细胞对脂多糖的反应、一氧化氮生物合成过程、C 型凝集素受体信号通路、IL-17 信号通路等生物过程及信号通路参与各种复杂的生物反应过程,发挥治疗 AS 的作用。因此本研究为 AS 的治疗提供了理论依据,但本研究基于网络药理学预测,仍需通过细胞实验(如 THP-1 巨噬细胞泡沫化模型)和动物实验(如 ApoE-/-小鼠)验证核心靶点及通路。
参考文献:
[1]TsaoCW,Aday AW,AlmarzooqZI,et al.Heart Disease and Stroke Statistics-2023 Update:A Report From the American Heart Association[J].Circulation,2023,147(8):e93-e621.
[2]Peng Kong,Zi Yang Cui,Xiao Fu Huang,et al.Inflammation and atherosclerosis: signaling pathways and therapeutic intervention[J].Signal Transduct Target Ther,2022 Apr 22,7(1):131.
[3]Jingyun Cheng,Hui Huang,Yu Chen,et al.Nanomedicine for Diagnosis and Treatment of Atherosclerosis[J].Adv Sci (Weinh),2023,10(36):e2304294.
[4]Yuanyuan Deng,Ruirong Tan,Fei Li,et al.Isorhynchophylline Ameliorates Cerebral Ischemia/Reperfusion Injury by Inhibiting CX3CR1-Mediated Microglial Activation and Neuroinflammation[J].Front Pharmacol,2021,12(12): 574793.
[5]Zhang YT,Cui YQ,Dai S,et al.Isorhynchophylline enhances Nrf2 and inhibits MAPK pathway in cardiac hypertrophy[J].Naunyn Schmiedebergs Arch Pharmacol,2020,393(2):203-212.
[6]韦贵云,许崇摇.钩藤碱和异钩藤碱抗高血压作用的研究进展[J].中国医药科学,2020,10(15):32-36.
[7]刘崇,刘亚婷,张壮,等.异钩藤碱减轻帕金森病小鼠多巴胺能神经元损伤的作用机制[J].安徽医药 2025,29(1):23-28.
[8]Xialin Zhu,Qingqing Hou,Ling Zhang,et al.Isorhynchophylline improves lipid metabolism disorder by mediating a circadian rhythm gene Bmal1 in spontaneously hypertensive rat[J].Phytother Res,2023,37(12):5991-6005.
[9]Meiyu Jin,Di Zhang,Lianwen Zheng,et al.Lipopolysaccharide and tyloxapol accelerate the development of atherosclerosis in mice[J].Lipids,2022,57:83–90.
[10]Hami Yu,Yujin Jin,Hyesu Jeon,et al.Protective effect of 6′ -Sialyllactose on LPS-induced macrophage inflammation via regulating Nrf2-mediated oxidative stress and inflammatory signaling pathways[J].Korean J Physiol Pharmacol,2024,1;28(6):503-513.
[11]Roman Roy,Joshua Wilcox,Andrew J Webb,et al.Dysfunctional and Dysregulated Nitric Oxide Synthases in Cardiovascular Disease: Mechanisms and Therapeutic Potential[J].Int J Mol Sci,2023,24(20):15200.
[12]MartaAleksandrowicz,Marek Konop,Mateusz Rybka,et al.Dysfunction of Microcirculation in Atherosclerosis: Implications of Nitric Oxide,Oxidative Stress,and Inflammation[J].Int J Mol Sci,2025,26(13):6467.
[13]Jeanette Owusu,Eugene Barrett.Early Microvascular Dysfunction:Is the Vasa Vasorum a "Missing Link" in Insulin Resistance and Atherosclerosis[J].International journal of molecular sciences 2021,22(14):7574.
[14]史云聪,郭艺芳.2 型糖尿病和动脉粥样硬化性心血管病的关系[J].心血管病学进展,2020,5:41(5).
[15]田惠铭,李霞.血管内皮生长因子与动脉粥样硬化关系的研究进展[J].医学综述.2023,29(22):4815-4820.
[16]岑团,黄照河,刘燕.血管内皮生长因子与动脉粥样硬化斑块的研究进展[J].右江医学.2021,49(6).
[17]Lei Nie,Xuying Xiang,Cheng Wen,et al.The Role of Lipid Subcomponents in the Development of Atherosclerotic Plaques[J].Rev Cardiovasc Med,2023,24(5):139.
[18]徐玉顺,郑丹,宋伟.C 型凝集素识别受体 2 调控动脉粥样硬化平滑肌细胞增殖和表型转化的机制研究[J]. 医学研究杂志,2021,50(3):80-83.
[19]Marie Robert,Pierre Miossec,Arnaud Hot.The Th17 Pathway in Vascular Inflammation:Culprit or Consort?[J].Front Immunol,2022,11(13):888763.
[20]Marie Robert,Pierre Miossec.Effects of Interleukin 17 on the cardiovascular system[J].Autoimmun Rev,2017,16(9):984-991.
[21]BijianWang,Taidou,Jiang,YaoyuQi,et al.AGE-RAGE Axis and Cardiovascular Diseases: Pathophysiologic Mechanisms and Prospects for Clinical Applications[J].Cardiovasc Drugs Ther,2024 Nov,5.






 京公网安备 11011302003690号
京公网安备 11011302003690号


