
- 收藏
- 加入书签
大麦气孔相关基因HvStomagen的克隆及其不同胁迫下的表达分析
摘要:气孔是植物叶片表皮上由一对保卫细胞构成的小孔,其主要作用包括气体交换、水分蒸腾和光合作用的调节。Stomagen作为一种分泌小肽,在植物气孔发育中起着关键的正向调控作用。为探究Stomagen在大麦响应逆境的作用,本研究以单子叶作物大麦Morex为材料,对大麦HvStomagen基因进行克隆,对其理化性质和蛋白结构等进行生物信息学分析,通过施加ABA、PEG6000模拟干旱胁迫、高温胁迫、低温胁迫鉴定其功能。结果表明,大麦HvStomagen基因编码区长506 bp,由122 个氨基酸构成,蛋白分子式为C580H921N169O181S12,存在信号肽,是碱性亲水不稳定分泌蛋白。大麦HvStomagen基因属于EPF/EPFL因子家族中的EPFL9亚家族。生物信息学预测HvStomagen基因定位于高尔基体。系统进化树显示大麦HvStomagen与小麦、节节麦等禾本科作物的Stomagen亲缘关系相对较近。大麦HvStomagen基因表达量受到干旱、ABA、高温和低温的影响,20%PEG6000模拟干旱胁迫处理下大麦HvStomagen基因的表达量随胁迫时间变化皆存在显著性差异;ABA溶液处理下,大麦HvStomagen基因表达明显被抑制,但同期对照组的基因表达量呈上升趋势。45℃高温与4℃低温处理下大麦HvStomagen基因表达量呈整体下降趋势,在3h、5h、7h时差异显著。推测其参与ABA介导的气孔发育网络途径和大麦逆境胁迫响应。本研究将为Stomagen基因在单子叶植物中的进一步的功能鉴定及气孔发育分子机制完善提供依据。
关键词:大麦;气孔发育;HvStomagen基因;基因克隆;逆境胁迫
前言
禾本科作物大麦(Hordeum vulgare)作为世界第四大禾谷类作物,在全世界被广泛种植。经过长期自然选择和人工选择演变,进而拥有多样的遗传特性,是作为抗逆生理研究重要种质资源。气孔是植物进化过程中保留的一种微观结构,由一对环绕中心孔洞的保卫细胞构成,是植物与大气进行水气交换的阀门,主要负责调节植物光合作用与蒸腾作用并通过调节开度响应逆境胁迫。
气孔发育受到多种内外源性因素的调控。内源性因素包括植物激素(如生长素、脱落酸、赤霉素等),EPF家族肽激素及其他转录因子和信号分子等。气孔蛋白Stomagen属于EPF家族,是一种特殊的分泌肽激素,是迄今为止唯一不表达于表皮细胞,而表达于叶肉细胞的气孔发育正调控因子。生长素通过核受体介导的生长素信号转导途径来促进响应因子ARF家族对下游基因的转录调控而参与调控植物生长发育,直接调控上游正调控因子编码基因Stomagen的表达,从而负调控气孔发育。Stomagen通过与细胞膜上的TMM/ERF形成配体-受体对,参与MAPK信号途径,从而调控气孔发育的关键转录因子的活性,进而影响气孔发育。气孔蛋白在促进气孔发育起始和气孔前体细胞分化中具有双重功能,通过对玉米ZmSTOMAGEN研究发现该基因的缺失导致了气孔发育的缺陷,包括气孔密度和指数的显著降低,以及光合作用效率和蒸腾速率的下降等。研究表明,Stomagen在单子叶作物和双子叶植物进化中产生了明显差异,可能与基因的表达调控以及蛋白功能的活化机制有关。EPF家族在基因结构上均由3个外显子和2个内含子构成,编码的蛋白也均属于不稳定的疏水性蛋白,且存在信号肽结构和C端保守的6个半胱氨酸残基,这些特性能使其能够响应特定的信号并快速调整气孔发育状态,以适应环境变化。Stomagen在不同植物类群中的进化具有复杂性,其结构和功能的差异可能与植物对抗逆适应性的需求有关。Stomagen基因的进化不仅受到遗传因素的影响,还受到逆境胁迫压力的选择。在植物激素调控与逆境胁迫不同的条件下,大麦气孔发育过程中Stomagen基因的功能可能会存在显著差异。
因此,本研究克隆了大麦HvStomagen基因并进行生物信息学分析;初步分析和总结了该基因在面对干旱胁迫、高温胁迫、低温胁迫时的相对表达量,旨在为Stomagen基因进一步的功能研究和应用奠定基础,也为单子叶植物气孔发育分子机制完善提供依据
1.材料和方法
1.1 实验材料
本实验采用大麦Morex品种为材料。
1.2 大麦材料处理及RNA的提取
将春化处理后的大麦种子置于平铺湿润棉花培养皿至发芽,3d后将其分为未处理组和A处理组(20%PEG6000溶液模拟干旱处理)、B处理组(ABA溶液处理)、C处理组(45℃高温处理)、D处理组(4℃低温处理),每组为10株,处理时间分别为 1h,3h,5h,7h,9h,11h。使用Plant Total RNA Isolation Kit 试剂盒(生工,上海)进行RNA提取。
1.3反转录cDNA模板
使用M-MuLV Reverse Transcriptase试剂盒(生工,上海)将上述提取的RNA反转录为cDNA,作为后续基因克隆的模板。
1.4大麦HvStomagen基因的克隆
使用NCBI (http://www.ncbi.nlm.nih.gov/gorg/gorf.html)查找Stomagen基因编码序列,通过Primer3Plus网站设计HvStomagen基因特异性引物见表 2,用上述得到的cDNA模板扩增Stomagen基因的编码区并进行PCR扩增,PCR扩增体系为ddH2O(8μL)、2×PrimeSTAR Max Premix(10μL)、引物Stomagen-R3(1μL)、引物Stomagen-F3(1μL)、cDNA模板(1μL),体系大小为20μL。PCR扩增反应程序为98℃(90s);98℃(10s),58℃(30s),72℃(90s)30个循环;72℃(60s);22℃保温。
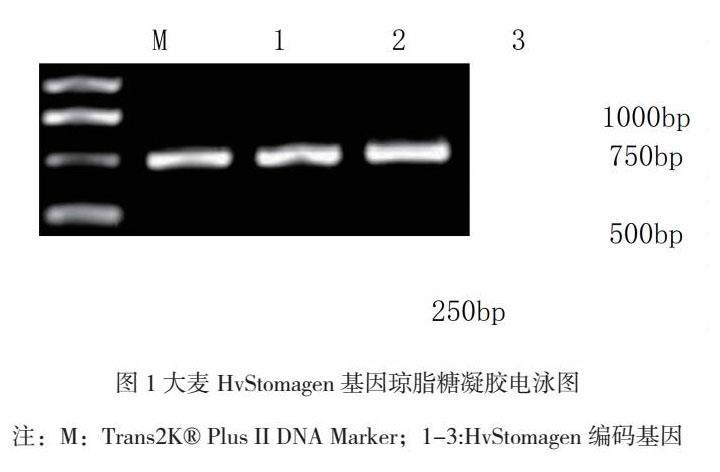
PCR结果经1%琼脂糖凝胶电泳验证后,Trans2K® Plus II DNA Marker对比目的条带,通过Gel Extraction Kit试剂盒回收目标DNA片段,将胶回收产物连接至pUCm-T克隆载体后将其转化大肠杆菌DH5α,阳性筛选培养后,使用天根科技有限公司质粒小型提取盒提取质粒,所得质粒送至生工生物工程(上海)股份有限公司进行测序,获取目的基因序列。
1.5生物信息学分析
软件及其用途见表 1
1.6 qRT-PCR检测大麦 HvStomagen基因的表达模式
荧光定量特异性引物见表2,用ABI7500 Fast qRT-PCR荧光定量仪进行三次试验和数据分析,检测大麦HvStomagen基因正常条件下和ABA溶液,45度高温,4度低温,模拟干旱(20%PEG6000)处理条件下1h,3h,5h,7h,9h,11h的表达量变化;检测过表达大麦HvStomagen的拟南芥叶片中的HvStomagen基因表达量变化,采用2 - ΔΔCt法分析数据。
1.7数据处理
本研究中的所有实验数据均通过三次独立重复实验获取,并计算其平均值作为最终分析结果。数据的图表绘制和统计分析分别借助Prism 10、Excel及IBM SPSS Statistics 25等工具完成。在差异显著性评估方面,采用独立样本t检验法进行判断,其中*表示**P < 0.01三星号(***p<0.01)和单星号(*0.01≤p≤0.05)分别表示不同水平的差异显著性。对于多组数据间的比较,则应用字母标记法来区分各组间的统计学差异。
2.结果与分析
2.1HvStomagen基因及氨基酸序列分析
以大麦Morex种子萌发第一片真叶的cDNA为模板,PCR法克隆得到HvStomagen基因编码区,得到长度为506bp的目的片段序列(图1),与Morex的cDNA进行序列比对(图2)。
生物信息学分析表明,大麦 HvStomagen蛋白分子式为C580H921N169O181S12,分子量为13542.44Da,理论等电点为7.58,不稳定指数为66.88,该蛋白为不稳定蛋白。基因编码区包含122个氨基酸,富含8个半胱氨酸,酸性残基(Asp + Glu)总数11个,碱性残基(Arg + Lys+His)总数17个,推测该蛋白为碱性蛋白。亲脂性指数为70.41,亲水性总平均值-0.425,推测为亲水性蛋白。该蛋白不存在跨膜结构域,但存在信号肽,推测其为分泌蛋白。
2.2大麦HvStomagen基因结构特征分析
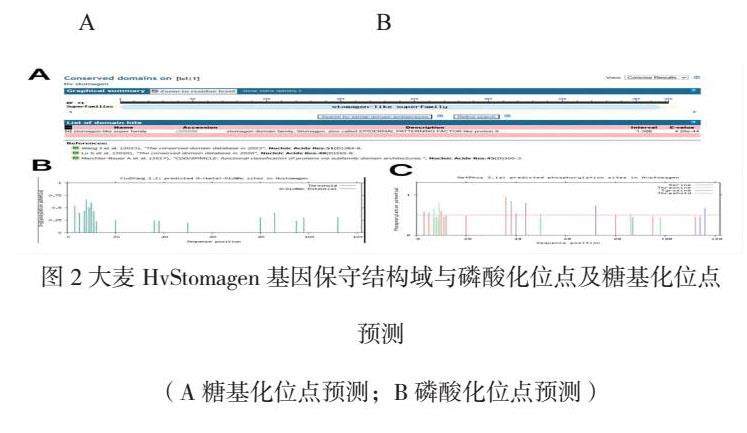
2.2.1大麦HvStomagen基因保守结构域与磷酸化位点及糖基化位点预测
保守结构域分析表明大麦HvStomagen基因属于EPF/EPFL因子家族中的EPFL9亚家族。糖基化位点(图2A)与磷酸化位点图(图2B)预测,说明该基因具有O-GlcNAc糖基化修饰作用与磷酸化修饰作用。
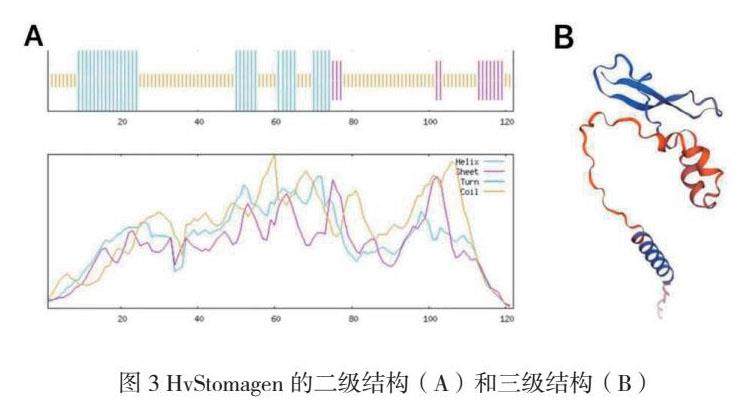
2.2.2大麦HvStomagen蛋白二级、三级结构预测
大麦HvStomagen蛋白二级结构主要由无规卷曲(77,63.11%)、α-螺旋(32,26.23%)和延伸链(13,10.66%)构成(图3A)。预测蛋白三维结构(图3B)由一个环和一个含有3个二硫键的折叠组成,其中两个反平行β-折叠通过一个14残基的环连接。
2.2.3大麦HvStomagen系统进化树分析
将大麦HvStomagen与34个植物(9个双子叶植物、25个单子叶植物)EPFL9序列比对后进行系统进化树分析,结果表明大麦HvStomagen与乌拉尔图小麦、普通小麦、节节麦、野生二粒小麦存在较高的同源性,与双子叶植物亲缘关系较远(图5)。
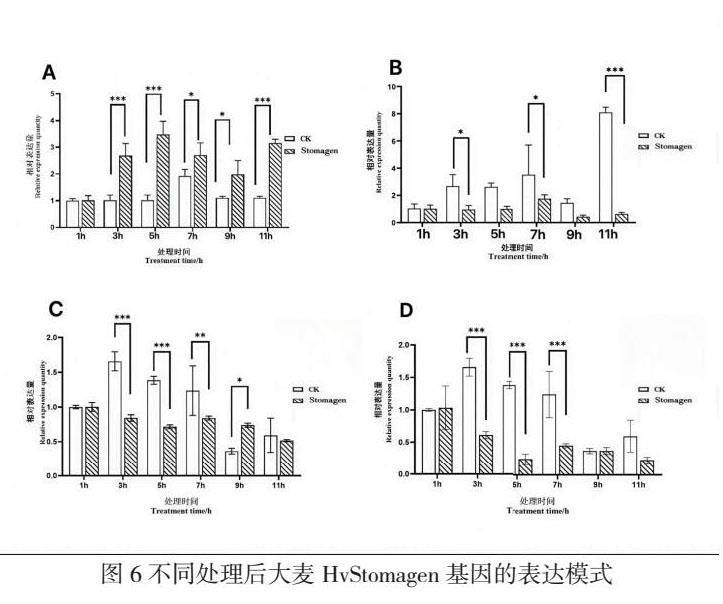
2.3不同处理后大麦HvStomagen基因的表达模式
以未处理组和A处理组、B处理组、C处理组、D处理组培养至萌发的第一片真叶的cDNA为模板,qRT-PCR三次重复结果表明,20%PEG6000模拟干旱胁迫处理下大麦HvStomagen基因的表达量随胁迫时间变化皆存在显著性差异(图6A)。对照处理组表达量无显著变化,在7h时表达量上升后又恢复,在20% PEG6000处理5 h时大麦HvStomagen基因表达量达到最高峰;ABA处理下(图6B),大麦HvStomagen基因表达明显被抑制,但同期CK组的基因表达量呈上升趋势。45℃高温(图6C)与4℃低温处理下(图6D)大麦HvStomagen基因表达量呈整体下降趋势,在3h、5h、7h时差异显著。
3.讨论
气孔的调节机制对于植物的生长发育、水分利用效率以及对环境变化的适应具有重要意义。气孔的发育与调节受到复杂的分子调控机制的影响,包括转录因子、信号肽以及植物激素等。这些调控机制确保了气孔在不同环境条件下的适当调节,以适应环境变化并维持植物的正常生理功能。
EPF/EPFL因子家族主要包括EPF1、EPF2和EPFL9/Stomagen等基因,是一类富含半胱氨酸的分泌型小肽,该基因定位于大麦5H染色体长臂且在植物的生长发育和形态建成过程中发挥重要作用。半胱氨酸是植物应对环境压力的重要分子,半胱氨酸在植物生长与逆境响应中主要通过其抗氧化功能发挥作用,帮助植物抵抗由环境压力引起的氧化损伤,并可能通过影响相关酶的活性或稳定性间接参与逆境响应过程。大麦HvStomagen基因编码区富含8个半胱氨酸,在模拟干旱胁迫条件下表达量整体产生显著性上升的原因可能是因胁迫下释放了大量的活性氧(ROS),自噬作用需要通过半胱氨酸分子维持ROS稳态。
EPF/EPFL家族蛋白的结构特征也揭示了它们的功能多样性,EPF1-EPF2和EPFL9在气孔发育过程中表现出拮抗作用,研究表明AtEPF1/EPF2-like肽在其环区形成额外的二硫键,这些区域比AtEPFL9/Stomagen-like肽显示出更大的灵活性,说明EPFL9/Stomagen亚家族通过不同的机制影响植物调节能力。在小麦中,全基因组水平共鉴定到EPF/EPFL基因家族成员为35个,含有1~4个外显子,分布在19条染色体上。与其他物种Stomagen蛋白构建进化树比对发现,大麦HvStomagen基因与小麦的EPF/EPFL同源性较高,进化中存在保守性。研究表明,EPFL9亚家族基因不仅在正常条件下调节气孔密度,也在植物适应环境胁迫中发挥关键作用。
大麦HvStomagen基因存在17个O-糖基化位点(11个Ser,6个Thr)、14个磷酸化位点(6个Ser ,4个Thr,4个Tyr)。研究表明,糖基化修饰与磷酸化修饰同样也在各类胁迫的响应中扮演重要角色。糖基化作为一种代谢途径,通过参与某些化合物(如氨基酸、酚类、激素、多胺、抗氧化剂)的合成或调节其表达,从而增强植物对胁迫的耐受性。
从气孔优化理论和cohesion-tension理论的角度来看,胁迫条件下,由于根到叶的水分运输受到限制,植物可能会通过增加气孔数量来补偿这种水分运输的不足,从而保持一定的光合作用和生长速率。有研究表明,大麦HvStomagen基因会通过增加气孔密度来调节气体交换和水分蒸腾过程。在高温、低温胁迫情况下,ABA激素的水平都会增加,在外源ABA处理下,大麦HvStomagen基因表达量下降,同Cutler S, 等人研究结果一致,Stomagen基因表达抑制,促进保卫细胞内源NO和H2O2的形成来诱导气孔关闭。气孔为了保证自身含水量,会减少大麦HvStomagen基因表达量促使气孔关闭,减少水分蒸腾。在高温条件下,植物体内的水分蒸发加快,导致叶片水势下降。为了维持细胞的正常生理活动和避免细胞失水过度,通过关闭气孔以保持细胞内外的水分平衡。而低温条件下,水分容易通过气孔蒸发,导致植物体内水分减少,从而增加细胞膜的脆性,最终可能导致细胞破裂和组织损伤。气孔密度减少可以通过减少水分的蒸发来保护植物免受冻害,帮助植物维持细胞的正常功能和结构完整性。本研究结果同样如此,研究中4度低温处理下,大麦HvStomagen基因表达量下调更加明显。植物通过调节气孔密度和开闭来适应环境变化的能力,以此增强干旱等非生物胁迫的耐受性与抗逆性。
参考文献
[1] 郭呈宇,伊风艳,房永雨,等.99份大麦种质资源表型性状遗传多样性分析[J].北方农业学报,2023,51(4):1-10.
[1] GUO C Y, YI F Y, FANG Y Y, et al. Analysis of genetic diversity of phenotypic traits in 99 barley germplasm resources[J]. Journal of Northern Agricultural Sciences, 2023, 51(4): 1-10.
[2] 栾海业,朱琳洁,李钰,等.大麦籽粒相关性状全基因组关联分析[J/OL].浙江农业学报,2024:997-1002[2024-04-25].
[2] LUAN H Y, ZHU L J, LI Y, et al. Genome-wide association analysis of barley grain related traits[J/OL]. Journal of Zhejiang Agricultural Sciences, 2024: 997-1002[2024-04-25].
[3] 程晓彬,赵钢,薛文韬,等.约旦野生二棱大麦在川西高原的物候期和农艺性状分析[J].西南农业学报,2016,29(5):1027-1031.
[3] CHENG X B, ZHAO G, XUE W T, et al. Analysis of phenophase and agronomic traits of Jordan wild two-rowed barley in western Sichuan Plateau[J]. Southwest China Journal of Agricultural Sciences, 2016, 29(5): 1027-1031.
[4] 王青,刘聪聪,何念鹏,等.内蒙古高原植物气孔性状的空间变异及其适应机制[J].生态学报,2023,43(9):3766-3777.
[4] WANG Q, LIU C C, HE N P, et al. Spatial variation and adaptation mechanisms of stomatal traits in plants in Inner Mongolia Plateau[J]. Acta Ecologica Sinica, 2023, 43(9): 3766-3777.
[5] 王碧霞,曾永海,王大勇,等.叶片气孔分布及生理特征对环境胁迫的响应[J].干旱地区农业研究,2010,28(2):122-126.
[5] WANG B X, ZENG Y H, WANG D Y, et al. Responses of leaf stomatal distribution and physiological characteristics to environmental stress[J]. Agricultural Research in the Arid Areas, 2010, 28(2): 122-126.
[6] 周丽娟,陈尔娟,韩笑,等.激素与气孔发育研究进展[J].西北植物学报,2015,35(4):845-851.
[6] ZHOU L J, CHEN E J, HAN X, et al. Research progress on hormones and stomatal development[J]. Acta Botanica Boreali-Occidentalia Sinica, 2015, 35(4): 845-851.
[7] 张静懿.生长素调控气孔发育的功能和作用分子机理的研究[D].上海:上海交通大学,2017.
[7] ZHANG J Y. Study on the function and molecular mechanism of auxin regulating stomatal development[D]. Shanghai: Shanghai Jiao Tong University, 2017.
[8] 陈少平.油菜BnA.EPF2和BnA.EPFL9基因调控气孔发育的功能分析[D].武汉:华中农业大学,2018.
[8] CHEN S P. Functional analysis of BnA.EPF2 and BnA.EPFL9 genes regulating stomatal development in rape[D]. Wuhan: Huazhong Agricultural University, 2018.
[9] JEZJ.Molecularcontrolsinplanthormonesignaling[J].TheFASEBJournal,2016,253(3):253-263.
[10] 陈青云.玉米中STOMAGEN-Like基因调控气孔发育的功能研究[D].南宁:广西大学,2018.
[10] CHEN Q Y. Functional study on the regulation of stomatal development by STOMAGEN-like gene in maize[D]. Nanning: Guangxi University, 2018.
[11] 樊宪伟,韦葳,廖权能,等.气孔蛋白同源物在单、双子叶植物中的生物信息学分析[J].基因组学与应用生物学,2013,32(6):752-760.
[11] FAN X W, WEI W, LIAO Q N, et al. Bioinformatics analysis of stomatal protein homologues in monocotyledonous and dicotyledonous plants[J]. Genomics and Applied Biology, 2013, 32(6): 752-760.
[12] RAVENJA.Selectionpressuresonstomatalevolution[J].NewPhytologist,2002,153(3):371-386.
[13] 刘婧,王宝山,谢先芝.植物气孔发育及其调控研究[J].遗传,2011,33(2):131-137.
[13] LIU J, WANG B S, XIE X Z. Research on plant stomatal development and its regulation[J]. Journal of Heredity, 2011, 33(2): 131-137.
[14] 杨天乐,吴峰峰,刘涛,等.作物气孔的作用及其影响因素的研究进展[J].北方园艺,2020,(3):143-148.
[14] YANG T L, WU F F, LIU T, et al. Research progress on the function and influencing factors of crop stomata[J]. Northern Horticulture, 2020, (3): 143-148.
[15] 高静.作物气孔对酵母免疫响应调节水分利用效率及其信号机制研究[D].杭州:浙江大学,2014.
[15] GAO J. Study on the regulation of water use efficiency and its signaling mechanism by crop stomata in response to yeast immune response[D]. Hangzhou: Zhejiang University, 2014.
[16] 商业绯,李明,丁博,等.生长素调控植物气孔发育的研究进展[J].植物学报,2017,52(2):235-240.
[16] SHANG Y F, LI M, DING B, et al. Research progress of auxin-regulated stomatal development in plants[J]. Chinese Bulletin of Botany, 2017, 52(2): 235-240.
[17] 崔国新,韩宝达,赵潇男,等.气孔发育及其调控[J].植物生理学报,2012,48(9):829-836.
[17] CUI G X, HAN B D, ZHAO X N, et al. Stomatal development and its regulation[J]. Plant Physiology Journal, 2012, 48(9): 829-836.
[18] ZHUJK.Saltanddroughtstresssignaltransductioninplants[J].AnnualReviewofPlantBiology,2002,53:247-273.
[19] THOMASHOWMF.Plantcoldacclimation:freezingtolerancegenesandregulatorymechanisms[J].AnnualReviewofPlantPhysiologyandPlantMolecularBiology,1999,50:571-599.
[20] FAROOQM,WAHIDA,KOBAYASHIN,etal.Plantdroughtstress:effects,mechanismsandmanagement[J].AgronomyforSustainableDevelopment,2011,29(1):185-212.
[21] SINGHD.PlantgrowthresponsesandprolineaccumulationundersalinitystressinthespeciesoffamilyMolguineaeinIndianThardert[J].EuropeanChemicalBulletin,2023,12(S5):2599-2616.
[22] QIH,LEIX,WANGY,etal.14-3-3proteinscontributetoautophagybymodulatingSINAT-mediateddegradationofATG13[J].PlantCell,2022,34(12):4857-4876.
[23] WANGS,WANGW,CHENJ,etal.Comprehensiveidentificationandexpressionprofilingofepidermalpatternfactor(EPF)genefamilyinoilseedrape(BrassicanapusL.)undersaltstress[J].Genes,2024,15(7):912.
[24] 魏迪,常平,刘佳熠,等.小麦EPF/EPFL基因家族的全基因组鉴定及TaEPF1-2B与气孔性状的关系分析[J].麦类作物学报,2021,41(11):1317-1329.
[24] WEI D, CHANG P, LIU J Y, et al. Genome-wide identification of the wheat EPF/EPFL gene family and analysis of the relationship between TaEPF1-2B and stomatal traits[J]. Journal of Triticeae Crops, 2021, 41(11): 1317-1329.
[25] ZHAOY,LYUAM,CHENG,etal.STOMAGEN-likeregulatesstomatalgenerationcausingincreasedwateruseefficiencyduringC4evolution[J].bioRxiv,2020:2020.11.10.377317.
[26] WUQ,LIZ,LIUJ,etal.Decipheringtheatlasofpost-translationalmodificationinsugarcane[J].JournalofAgriculturalandFoodChemistry,2023,71(40):14510-14517.
[27] SANVISENSN,LAOJ.Proteinpost-translationalmodificationsandtheDNAdamageresponse[J].CellCycle,2016,15(7):892-900.
[28] XUY.Advancesonthebiosynthesispathwaysandmolecularregulationmechanismofseveralimportantdefensivesubstancesinplantsecondarymetabolism[J].JournalofIntegrativePlantBiology,2013,55(4):285-289.
[29] NOVICKKA,MINIATCF.Droughtlimitationstoleaf-levelgasexchange:resultsfromamodellinkingstomataloptimizationandcohesion-tensiontheory[J].Plant,Cell&Environment,2016,39(3):583-596.
[30] KONDOT,KAJITAR,MIYAZAKIA,etal.Stomataldensityiscontrolledbyamesophyll-derivedsignalingmolecule[J].PlantandCellPhysiology,2010,51(1):1-8.
[31] SOJKARE.Stomatalclosureinoxygen-stressedplants[J].PlantPhysiology,1992,100(1):269-280.
[32] CUTLERSR,RODRIGUEZPL,FINKELSTEINRR,etal.Abscisicacid:emergenceofacoresignalingnetwork[J].AnnualReviewofPlantBiology,2010,61:651-679.
[33] 韩燕,佘小平.NO,H₂O₂介导根系渗透胁迫和脱落酸诱导的气孔关闭[J].陕西师范大学学报(自然科学版),2007,35(4):83-87.
[33] HAN Y, SHE X P. NO and H₂O₂ mediate stomatal closure induced by root osmotic stress and abscisic acid[J]. Journal of Shaanxi Normal University (Natural Science Edition), 2007, 35(4): 83-87.
[34] THOMPSONDS,WILKINSONS,BACONMA,etal.Multiplesignalsandmechanismsthatregulateleafgrowthandstomatalbehaviourduringwaterdeficit[J].JournalofExperimentalBotany,1997,48(SpecialIssue):303-313.
[35] WILKINSONS,CLEPHANAL,DAVIESWJ.Rapidlowtemperature-inducedstomatalclosureoccursincold-tolerantCommelinacommunisleavesbutnotincold-sensitivetobaccoleaves,viaamechanismthatinvolvesapoplasticcalciumbutnotabscisicacid[J].PlantPhysiology,2001,126(4):1566-1578.
作者简介:潘治锦(2003.04—),男,汉族,天津人,天津农学院本科在读,研究方向:大麦分子育种
谢晓东*(通讯作者) 陈小强*(通讯作者)
基金项目:河北省高等学校科学技术研究项目(YJZ2004001),天津市大学生创新创业训练计划项目(202410061102), 天津市科技计划项目(22ZXZYSN00020),天津市科技计划项目(22ZYCGSN00020),东西部科技协作专项(津甘合作、鲁甘合作)(24CXNL004)









 京公网安备 11011302003690号
京公网安备 11011302003690号


