
- 收藏
- 加入书签
分光光度法测定破壁灵芝孢子粉中总三萜含量研究
摘要:目的:为建立能够准确测定破壁灵芝孢子粉中总三萜含量的方法。方法:称取适量样品于50 mL容量瓶中,加入约30 mL氯仿,超声提取约30 min,离心10 min,精密移取1.0 mL上清液转入10 ml的比色管里,沸水浴挥干,冷却后精密加入0.4 mL 5%香草醛-冰乙酸溶液,再精密加入1.0mL高氯酸,充分混匀。将比色管置60 ℃水浴中加热15 min,取出,冰水浴冷却后,精密加入冰乙酸5.0 mL摇匀,放置15 min后于548nm波长下进行测定。结果:熊果酸标准溶液在20~160 μg质量浓度范围内线性良好,相关系数r2为0.9992,3个浓度水平的加标回收率在90.3~101.2%之间,相对标准偏差(n=3)在0.02~0.64%之间,精密度的相对标准偏差(n=6)为0.06%,方法检出限为0.7822 μg,定量限为2.3466 μg。结论:该方法操作简便,条件明确,测试结果准确度高,适用于破壁灵芝孢子粉中总三萜含量的测定。
关键词:破壁灵芝孢子粉;总三萜;分光光度法;
0 引言
灵芝(Ganoderma lingzhi)属于担子菌门、担子菌纲、非褶菌目、灵芝科、灵芝属 [1,2]。灵芝最早在《淮南子·修务训》中被载入[3,4],分类为:青芝、赤芝、黄芝、紫芝等六种,并被列为草部上品之首[5-9]。其中赤芝和紫芝为《中华人民共和国药典》2000年版一部首次收载的品种[10] 。灵芝具有较高的药用价值,对人体五脏都有良好的补益作用 [11]。目前市面上的灵芝制品有:破壁灵芝孢子粉、灵芝孢子粉片、灵芝孢子油、灵芝孢子油软胶囊等;其中以破壁灵芝孢子粉居多,同时破壁灵芝孢子粉也是一种重要的保健食品原料。
总三萜化合物是灵芝及其制品中的主要功效成分,具有多种生理活性[12]:如保肝护肝[13-14]、抗炎[15-16]、降血糖[17]、抗肿瘤[18]、抗氧化[19-20]、神经保护[21]等多种药理活性,应用前景广泛,因此破壁灵芝孢子粉中三萜类化合物含量可作为评价其质量高低的一项重要指标。近年来灵芝三萜逐渐受到研究者的重视,相关报道日渐增多,灵芝三萜含量测定的方法主要包括高效液相色谱法以及紫外分光光度法。其中高效液相色谱法准确度高,但需要大量的高纯度三萜类化合物作为标准品,要分离获得高纯度具有代表性的三萜化合物对照品技术难度很大;分光光度法准确度不如高效液相色谱法,但能以目前自然界广泛存在的三萜化合物熊果酸、齐墩果酸作为对照品,目前破壁灵芝孢子粉中总三萜含量测定基本采用分光光度法。现有的定破壁灵芝孢子粉中总三萜含量的分光光度方法诸多条件存在不明确:如《保健食品理化及卫生指标检验与评价技术指导原则》(2020年版)(《评价技术2020版》)中使用了离心,但是并未明确离心的条件;《保健食品功效成分检测方法》(2011版)(《功效成分2011版》)中总三萜含量测试条件对样品的提取后:浑浊可过滤等[12],但并未定义如何判断浑浊。因破壁灵芝孢子粉极易产生悬浮,对相关步骤要求不明确从而影响测试结果的准确性,以及重现性差等问题。破壁灵芝孢子粉中总三萜含量的测定现为行业内公认的技术难点,因此亟需对测试方法进行优化,明确测试条件并验证方法的可靠性。
此研究主要针对破壁灵芝孢子粉中总三萜进行测定,使用分光光度法测定,通过对方法中挥干方式、除杂方式、水浴条件等进行优化,对所确立的方法线性范围、检出限与定量限、专属性、重复性、准确性、耐用性等开展大量试验,验证本方法的适用性、可靠性及优越性。最终确立能够对破壁灵芝孢子粉中总三萜含量进行准确测定的方法,从而有效突破行业内检测技术壁垒,为保健食品生产企业质量控制提供有力的技术支持。
1 材料与方法
1.1 主要材料与试剂
熊果酸标准品(纯度:99.0%,CAS:77-52-1,分子式:C30H48O3,相对分子量:456.68,中国食品药品检定研究院);乙酸乙酯、冰乙酸(分析纯,天津大茂试剂厂);氯仿(分析纯,广州化学试剂厂);高氯酸(优级纯,成都市科隆化学品有限公司);香草醛(分析纯,天津科密欧试剂有限公司)。
1.2主要仪器与设备
UV-1800紫外-可见分光光度计(岛津仪器苏州有限公司);ME204E、ME155DU分析天平(瑞士Mettler Toledo公司);HH-4恒温水浴锅(常州普天仪器制造有限公司);XWDS-1018ST超声波清洗器(东莞市万德盛自动化设备有限公司);L-530台式低速离心机(湖南冲康离心机有限公司)。
1.3 试验条件
1.3.1 溶液配制
熊果酸标准品溶液(100 μg/mL):精密称取熊果酸标准品10 mg,至于100 mL容量瓶中,用乙酸乙酯溶解并定容,充分混匀。
香草醛冰乙酸溶液(5%):精密称取香草醛试剂0.5g,用冰乙酸溶解并定容至10mL后摇匀。现配现用。
1.3.2 试样制备
称取试样控制在0.1 g,精密称定,于50 mL的容量瓶中,加氯仿约30 mL,超声处理约30 min,冷缺后,加氯仿至刻度,摇匀。离心10 min,取上清液为待测液。
1.3.3 标准曲线的制作
精密吸取标准溶液0.00、0.10、0.20、0.40、0.80、1.00 mL置比色管中,于沸水浴挥干,冷却后精密加入0.4 mL5%香草醛冰乙酸溶液,充分摇匀,再精密加入1.0 mL高氯酸溶液,混匀后移置水浴中60℃加热15 min,立即取出,冰浴冷却,精密加入冰乙酸5.0 mL摇匀,15 min后在比色皿中548 nm波长下测定吸光值;以吸光值作为纵坐标,以浓度为横坐标绘制出标准曲线。
1.3.4 试样溶液的测定
精密量取试样上清液1.0 mL置10 ml比色管中,于沸水浴挥干,冷却后精密加入0.4 mL5%香草醛冰乙酸溶液,旋转蒸发皿使其残渣完全溶解,再精密加1.0 mL高氯酸溶液,混匀后转移至10 mL具塞比色管中,放置于水浴中60℃加热15 min,取出,冰浴冷却后,精密加入冰乙酸5.0 mL摇匀,放置15 min,用比色皿于548 nm波长下测定试样溶液的吸光值,根据标准曲线得到的待测液中总三萜的浓度进行计算。
1.3.5数据处理
试样中总三萜含量按公式(1)计算:
Xi 为样品中总三萜含量(以熊果酸计),g/100g; Ci为根据标准曲线得到的待测液中总三萜质量浓度,μg;m为精密称取的样品质量,g;V1为试样定容总体积,mL;V2为测定用所移取的试样体积,mL。
使用Excel进行数据计算及图表绘制。
2 结果与分析
2.1 测定波长的确定
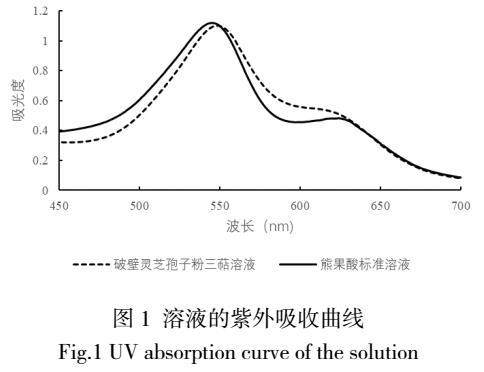
取熊果酸标准溶液和破壁灵芝孢子粉三萜提取溶液,经显色反应后,于450~700 nm波长范围内进行光谱扫描,获得吸收曲线见图1。由图1可知,发现熊果酸目标物质在548 nm波长处出现最大吸收峰,破壁灵芝孢子粉三萜在550 nm波长处有最大吸收,两者最大吸收波长较为接近,符合药典规定的试样最大波长允许误差范围,因此得到此方法的测定波长为548 nm。
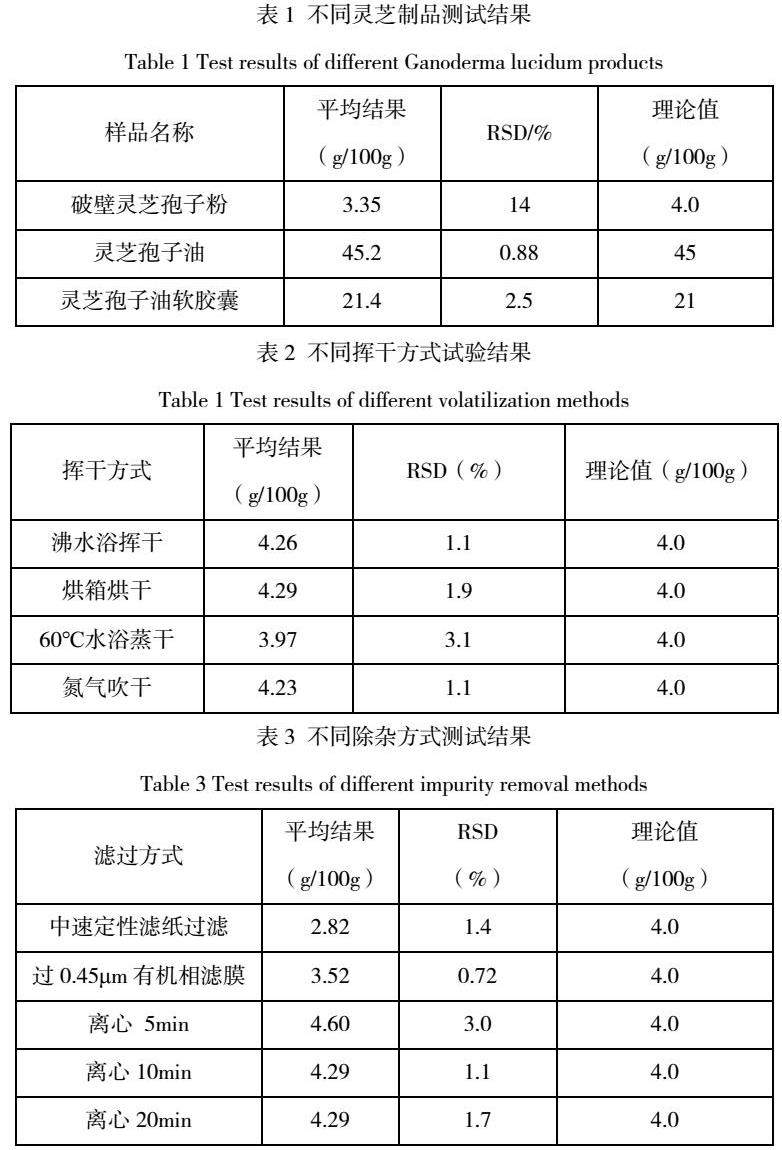
2.2 不同灵芝制品测试结果
通过选择不同类型的灵芝制品:破壁灵芝孢子粉、灵芝孢子油、灵芝孢子油软胶囊,依照《评价技术2020版》总三萜测试方法进行试验,结果如表1所示,通过测试结果可以看出:破壁灵芝孢子粉、灵芝孢子油、灵芝孢子油软胶囊的RSD分别为14%、 0.88%和2.5%,相比之下破壁灵芝孢子粉平行样间偏差较大,且与理论值对比,破壁灵芝孢子粉存在更大差异,故选择破壁灵芝孢子粉作为进一步研究基质。
2.3 方法优化
2.3.1 挥干方式的选择
挥干方式可分为:沸水浴挥干、烘箱烘干、60℃水浴蒸干、氮气吹干四种方式,选择破裂灵芝孢子粉为试样,通过实验表明:沸水浴挥干的测试RSD为1.1%,结果稳定,结果重现性相比其他方式更好如表2所示,以及比其他方式耗时较短,便于批量操作,效率更高。通过对比分析,沸水浴挥干的方式更优。
2.3.2 除杂方式的选择
除杂方式可分为:中速定性滤纸过滤、0.45 μm有机相滤膜过滤、4000 r/min离心(5 min、10 min、20 min)三种方式,选择破壁灵芝孢子粉为试样,通过实验表明:三种方式的结果都比较稳定,滤纸过滤和过0.45 μm有机滤膜的测试结果与理论结果有一定的偏差,离心的测试结果更符合理论结果如表3所示。通过对比分析,离心的方式更佳。在离心的时间选择:5 min、10 min、20 min。实验现象表明离心10min后上清液澄清无肉眼可见悬浮颗粒,从表3测试结果来看,继续离心测试结果无变换,说明离心10 min已达到彻底离心效果。
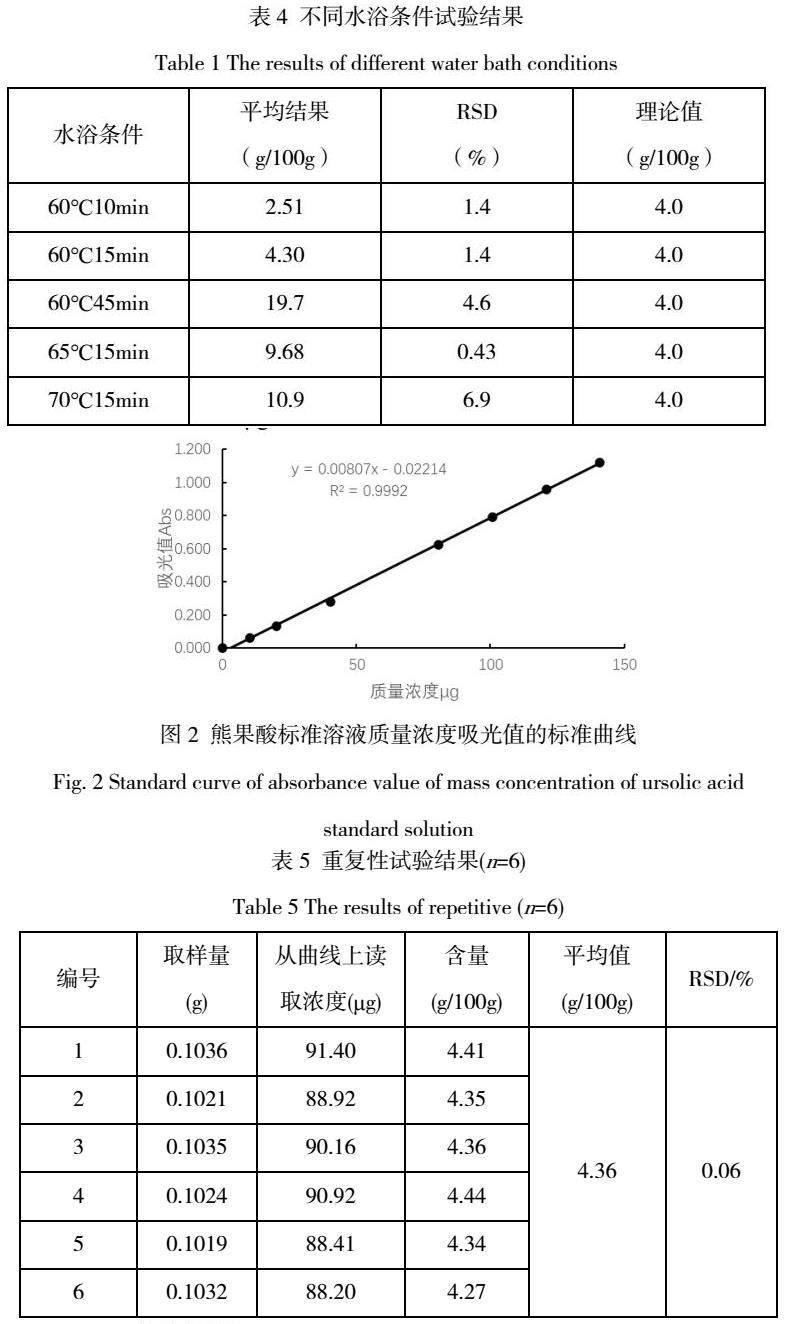
2.3.3 水浴条件的选择
通过考察不同水浴温度与不同时间的显色条件:60 ℃+10 min, 60 ℃ +15 min, 60 ℃ +45 min, 65℃ +15 min, 70 ℃+ 15 min,五组条件,考察反应温度和时间对测试结果的影响。测试结果见表4,可以发现结果与水浴温度和水浴时间呈正相关:温度控制在60℃不变的时,随着水浴时间增长测试结果变大;当水浴时间均控制在10 min时,随着水浴温度升高测试结果变大。在水浴条件的选择中,60 ℃+15 min条件下测试结果与理论值更接近,且偏差最小,因此选择此水浴条件。
2.4 方法验证
2.4.1 线性范围考察
分别精密吸取熊果酸标准品溶液按1.3.3操作进行测定吸光值,如图2所示,以熊果酸的质量浓度为X轴,以吸光值Y轴,进行线性回归,得到回归方程为:Y=0.00807X-0.02214,相关系数R2=0.9992,结果表明熊果酸标准品浓度在20~160μg范围内吸光值线性关系良好。
2.4.2检出限和定量限考察
通过分析20个独立试剂空白来计算方法检测限,通过计算得,标准偏差Sd=0.002104,检出限L=3·Sd/b=0.7822μg(b为斜率=0.00807),定量限= 3·L=2.3466μg。
2.4.3专属性实验
按照样品的组分特点,采用实验试剂羟丙基纤维素和葡萄糖混合(比例为8:2)配制阴性样品,同时做试剂空白,比较两组数据,空白溶液与阴性样品均无吸光值,专属性良好。
2.4.4 重复性试验
选取一款灵芝孢子粉精密称取0.1g(精确到0.0001g),称取6份按1.3.2方法进行样品处理,按2.3方法优化的条件进行6次重复性测试。测试结果如表5所示,样品中总三萜平均含量为4.36g/100g,RSD为0.06%,试验结果重复性良好。
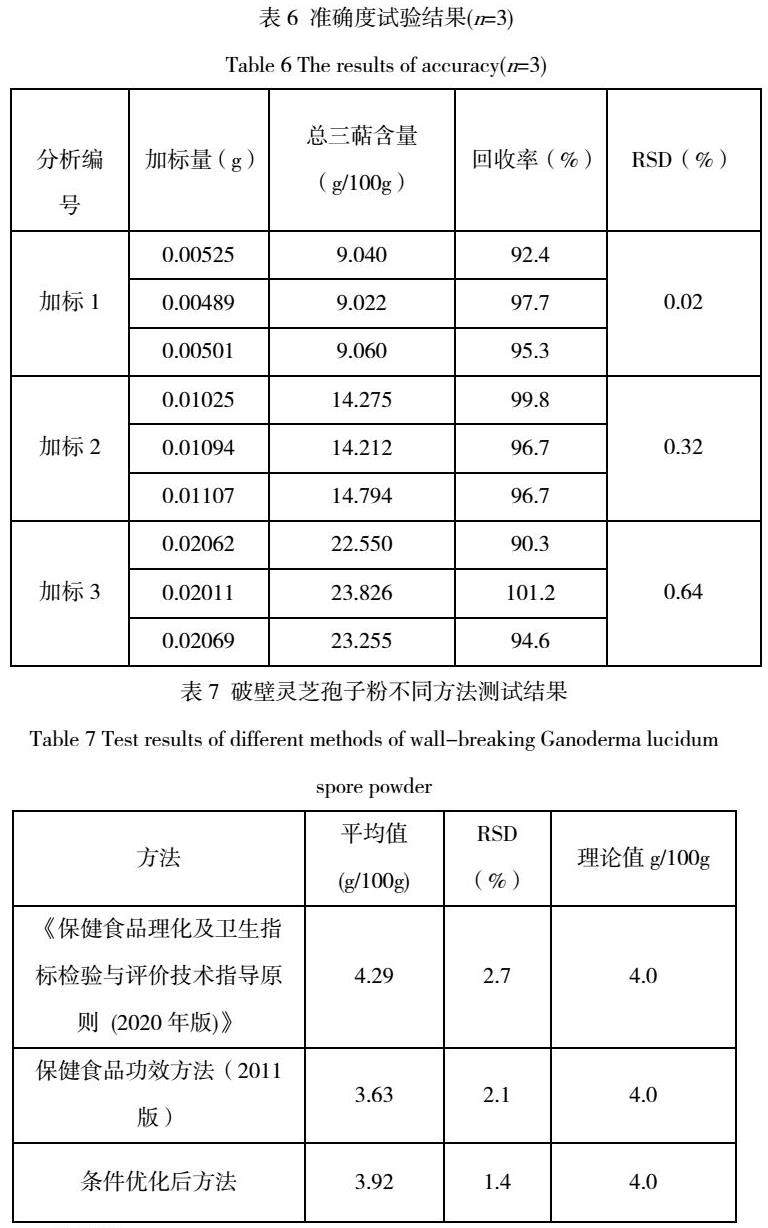
2.4.5准确度试验
精密称取上述同一灵芝孢子粉含量为4.36 g/100g的样品0.1g,加入低、中、高3个浓度水平的熊果酸标准品,考察方法的准确度。结果如表6所示,回收率在90.3~101.2%之间,RSD在0.02~0.64%,精密度和准确性均良好。
2.5 方法比对
选取破壁灵芝孢子粉作为测试样品,分别按照《评价技术2020版》、《《功效成分2011版》以及本研究对条件优化后的条件:沸水浴挥干溶剂、4000r/min 离心10min、水浴条件60℃ 15 min进行测试,测试结果如表10所示。优化条件后方法RSD为1.4%,同时通过对三种方法的测试结果与理论值的对比,优化后的方法与理论值更为接近,且操作简单,效率更高,相比其他方法具有明显的优越性。
3 结论
破壁灵芝孢子粉中总三萜含量测试由于已有方法中测试条件不明确,导致测试结果准确度低稳定性差。本研究通过在已有方法的基础上对方法中挥干方式、提取液除杂方式及水浴反应条件等进行优化并固定,从而确立破壁灵芝孢子粉总三萜测试的最佳条件为:沸水浴挥干、4000 r/min离心10 min以及60℃水浴反应15min。并进一步对所确立的方法通过方法学验证,对线性范围、精密度、专属性等进行验证,表明该方法测试结果准确可靠。同时此方法测试过程简便,条件明确,检测结果稳定准确,适用于破壁灵芝孢子粉测试总三萜含量测定,能够为灵芝制品中功效成分含量准确测定提供有力技术手段,为保健食品企业检测技术提升和产品质量控制提供技术支持。
参考文献
[1] 杨祝良. 基因组学时代的真菌分类学:机遇与挑战[J]. 菌物学报, 2013, 32(06): 931-946.
[2] 张彬彬. 南召县野生灵芝菌株的分离鉴定及其活性成分分析[D]. 河北工程大学, 2021.
[3] 林志彬. 灵芝研究与开发的历史、现状和未来[C]. 2004灵芝专题研讨会论文摘要集,中国北京: 2004: 6-7.
[4] 华敏. 中国灵芝饮食的历史变迁与发展展望[J]. 南宁职业技术学院学报, 2009, 14(06): 6-9.
[5] 贺新生. 《菌物字典》第10版菌物分类新系统简介[J]. 中国食用菌, 2009, 28(06): 59-61.
[6] 周选,围林娟. 中国野生灵芝资源的开发利用[J]. 食用菌学报, 1999, (01): 58-64.
[7] 张宏. 真菌分类学中的分子生物学技术点评[J]. 国外医学.皮肤性病学分册, 1997, (04): 215-219.
[8] 赵继鼎. 我国古籍中记载六芝的初步考证[J]. 微生物学通报, 1989, (03): 180-181.
[9] 李明焱. 《神农本草经》中灵芝的品属及功效——灵芝研究溯源及其评价[C]//.中医经典理论内涵与临床应用学术研讨会暨医史文献分会、中
医经典与传承研究分会(筹)学术年会文集.[出版者不详],2012:26-31.
[10] 钟显,程敏,林微微. 灵芝食用历史及安全性材料追溯[J]. 现代农业科技, 2020, (01): 80-83
[11] 贺新生. 《菌物字典》第10版菌物分类新系统简介[J]. 中国食用菌, 2009, 28(06): 59-61.
[12] 白鸿.保健食品功效成分检测方法[M].北京:中国中医药出版社,2011:58-59.
[13] 李鹏, 魏晓霞, 南婷婷, 等. 灵芝三萜酸对小鼠急性肝损伤的保 护作用[J]. 中国医院药学杂志, 2013, 33(23): 1914-1918. LI Peng, WEI Xiaoxia,
[14] 吴鑫, 周茜, 唐珊珊, 等. 灵芝总三萜对鹅膏毒肽中毒小鼠所致 肝损伤的保护作用研究[J]. 菌物学报, 2016, 35(10): 1244-1249. WU Xin, ZHOU
[15] 郝萌萌, 王金艳, 冯娜, 等. 灵芝子实体中不同极性的三萜体外 抗肿瘤及抗炎活性比较[J]. 菌物学报, 2019, 38(6): 917-925. HAO Mengmeng,
[16] SMINA T P, JOSEPH J, JANARDHANAN K K. Ganoderma lucidum total triterpenes prevent γ -radiation induced oxidative stress in Swiss albino mice in vivo[J]. Redox Report, 2016, 21(6): 254-261.
[17] CHEN S D, LI X M, YONG T Q, et al. Cytotoxic lanostane -type triterpenoids from the fruiting bodies of Ganoderma lucidum and their structure-activity relationships[J]. Oncotarget, 2017, 8(6): 10071- 10084.
[18] SMINA T P, NITHA B, DEVASAGAYAM T P A, et al. Ganoderma lucidum total triterpenes induce apoptosis in MCF-7 cells and at- tenuate DMBA induced mammary and skin carcinomas in experi- mental animals[J]. Mutation Research/Genetic Toxicology and En- vironmental Mutagenesis, 2017, 813: 45-51.
[19] TENG X Q, ZHANG W Q, SONG Y Y, et al. Protective effects of Ganoderma lucidum triterpenoids on oxidative stress and apoptosis in the spleen of chickens induced by cadmium[J]. Environmental Science and Pollution Research, 2019, 26(23): 23967-23980.
[20] HSU P L, LIN Y C, NI H, et al. Ganoderma triterpenoids exert an- tiatherogenic effects in mice by alleviating disturbed flow-induced oxidative stress and inflammation[J]. Oxidative Medicine and Cellular Longevity, 2018, 2018: 3491703.
[21] QIU J M, WANG X, SONG C G. Neuroprotective and antioxidant lanostanoid triterpenes from the fruiting bodies of Ganoderma atrum [J]. Fitoterapia, 2016, 109: 75-79.





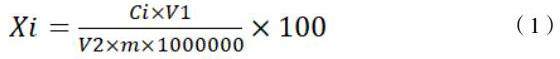
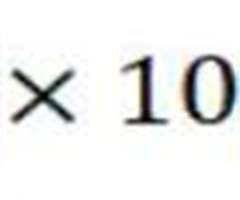

 京公网安备 11011302003690号
京公网安备 11011302003690号


