
- 收藏
- 加入书签
基于泡沫铜的表面增强拉曼光谱基底对肌酐快速检测的研究
摘要:目的 本文探讨了一种新型的检测方法—表面增强拉曼光谱法(Surface-Enhanced Raman Scattering,SERS),用于快速、灵敏地测定肌酐含量。方法 制备一种新型的三维(3D)多孔功能泡沫金属表面增强拉曼散射基底(CF/Au@Ag),该基底采用物理沉积法在泡沫铜骨架上附着金/银纳米粒子(Au@Ag NPs),制成CF/Au@Ag。该策略为局部等离子体材料的分布和构建提供了一种新途径,表现出更好的形貌调控能力和SERS活性。所开发的CF/Au@Ag具有大的表面积和丰富的热点,从而获得了优异的SERS性能。通过研究最佳沉积时间,制备最优CF/Au@Ag基底。采用对生理盐水中的肌酐进行无标记检测,测得特征峰线性相关系数。结果 制备最优CF/Au@Ag基底的最佳沉积时间为24 h,优化后的基底测得797 cm-1、974 cm-1和1446 cm-1特征峰的SERS强度与肌酐分子浓度的线性相关系数R2分别为0.9756、0.9610和0.9652。CF/Au@Ag基底对肌酐浓度的探测能力和精度在常温下较高。结论 制备最优CF/Au@Ag基底为肌酐分子浓度的准确探测提供了更可靠的方案。
关键词:最优基底;SERS;肌酐;灵敏检测
中图分类号:R473
Objective In this paper,a new detection method,Surfact-Enhanced Raman Scattering (SERS),was developed for the rapid and sensitive determination of creatinine content.Methods A novel three-dimensional (3D) porous functional metal foam surface enhanced Raman scattering substrate (CF/Au@Ag) was prepared.The substrate was attached with gold/silver nanoparticles (Au@Ag NPs) on the copper foam skeleton by physical deposition method,and CF/Au@Ag was prepared.This strategy provides a new way for the distribution and construction of local plasma materials,showing better morphology regulation and SERS activity.The developed CF/Au@Ag has a large surface area and abundant hot spots,thus obtaining excellent SERS performance.The optimum CF/Au@Ag substrate was prepared by studying the optimum deposition time.Creatinine in normal saline was detected without label and the linear correlation coefficient of characteristic peak was measured.Results The optimal deposition time of the optimized CF/Au@Ag substrate was 24 h.The linear correlation coefficients R2 of SERS intensity and molecular concentration of creatinine on 797 cm-1,974 cm-1 and 1446 cm-1 characteristic peaks were 0.9756,0.9610 and 0.9652,respectively.The ability and accuracy of CF/Au@Ag substrate to detect creatinine concentration were higher at room temperature.Conclusion The preparation of the optimal CF/Au@Ag substrate provides a more reliable method for the accurate detection of creatinine molecular concentration.
Keywords: optimal base,SERS,creatinine,ultrasensitive detection
1 引言
肌酐是评估肾功能和其他疾病的重要指标,肌酐水平不足表示肌肉萎缩、肝功能低下和体液流失。SERS是一种具有“指纹”特征,被认为是一种非侵入性技术,提供了拉曼光谱的选择性和在超低浓度下检测生物分子的高灵敏度。通过在纳米结构金属表面增强拉曼散射信号来检测低浓度的分子广泛应用于食品分析[1-3]、临床医学[4,5]、和药物代谢[6,7]等各个领域。在临床实验研究中,SERS已被用于检测多种人体代谢物。利用SERS技术成功检测到了尿液中的葡萄糖、肌酐和尿酸等代谢物[8,9],这对于糖尿病和肾脏疾病的早期诊断具有重要意义。此外,SERS还可以用于血液中的氨基酸、脂类和小分子代谢产物的分析[10],为肝功能异常和代谢综合征等疾病的诊断提供了有效手段。此前检测肌酐基底多为二维平面金/银基底[11,12],吸附肌酐能力和检测准确度不高。本文将介绍基于新型三维泡沫铜(CF/Au@Ag)基底快速检测肌酐含量的SERS方法,同时介绍了提高肌酐检测效率和提升定量分析能力的方法。CF/Au@Ag基底在肌酐检测中的应用为研究和临床诊断提供了一种新的SERS基底,更重要的是,它在临床上精确定量检测尿液中肌酐含量具有巨大潜力。
2 实验部分
2.1 试剂和化学品
肌酐(Cr,C4H7N3O,99%)、硝酸银(AgNO3,99.0%)、氨水(NH3·H2O,3wt%)、柠檬酸三钠(Na3C6H5O7)、盐酸(HCl,3mol)和无水葡萄糖(C6H12O6 ,99%)均购自国药集团化学试剂有限公司。所有溶液均用超纯Milli-Q水(电阻率为18.2 MΩ·cm)制备。
2.2 仪器设备
使用紫外可见近红外光谱仪对金属产物的共振吸收峰进行表征。使用配备785 nm激光器(Laser 785-5HS)和CCD探测器(iVac316)配备光栅光谱仪(Omini-λ5008i)获取SERS光谱。SERS测试使用了一台配备50倍物镜的共焦微探针拉曼光谱仪来获取信号。激发源为高功率的785 nm连续波二极管激光器,激光在不同样品表面的功率为30 W。每个样品扫描了10次,每次的累积时间为1秒。
2.3 Au@Ag的合成制备
将泡沫铜切割成1×1 cm2的正方形小块,将泡沫铜浸入3 mol/L HCl中超声处理5 min去除表面氧化层,使用去离子水将表面残留盐酸冲洗干净后将处理后的泡沫铜放在在乙醇中进行脱脂。
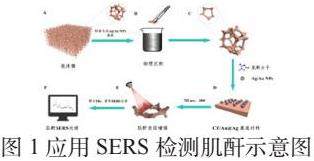
首先Ag NPs的制备采用Lee-Meisel法[13],待反应结束溶液自然冷却至室温后,以8000 r/min的速度离心30 min,除去上清液后的沉淀物稀释回20 mL。利用透射电子显微镜和紫外可见近红外光谱仪对制备的Ag NPs进行表征。Au-Ag核壳纳米结构(Au@Ag NPs)的制备可分为两个步骤。首先,以柠檬酸钠二水合物(C6H6Na3O7)为媒介,通过还原HAuCl4·3H2O制备Au NPs[14]。加热混合物30 min,直至溶液呈橙黄色,冷却至室温,避光保存一周以备后用,具体流程如图1(A-C)所示。
2.4 肌酐标准品的制备
配备标准肌酐溶液,称取11.31 mg的肌酐固体粉末并溶解在10 mL的生理盐水中,通过超声震荡使其均匀混合,制备出浓度为10–2 mol/L的肌酐溶液。随后,从该溶液中取出1 mL,并将其加入到9 mL的生理盐水中,稀释后得到浓度为10–3 mol/L的肌酐溶液。以此类推,通过稀释获得10-4 - 10-9 mol/L的肌酐溶液。Ag NPs使用台式离心机离心,Ag NPs以8000 r/min离心10 min。为了进行定量测量配制不同浓度的肌酐标准溶液,与银纳米颗粒溶液按1:1体积比混合,作为SERS检测的标准样品。稀释后分别得到浓度为2×10-3 - 2×10-9 mol/L的Cr/Ag样品,作为SERS检测的标准样品。将混合液滴放至CF/Au@Ag上,在25 ℃下干燥60 min,以促进Ag NPs与样品中的目标物质聚集。
2.5 分子组装与SERS检测
取10 μL标准肌酐溶液样品,然后进行SERS检测。测量来自随机位置的八个SERS光谱以获得平均光谱。对银纳米粒子的组装不仅提供了与生物分子的结合位点以增加其相容性,而且还使它们稳定以防止聚集。将不同浓度肌酐逐滴加入顶层,通过便携式拉曼光谱直接检测,激光功率为30 W,积分时间为5 s,具体流程如图1(D-F)所示。
3 结果
3.1 CF/Au@Ag的制备和表征
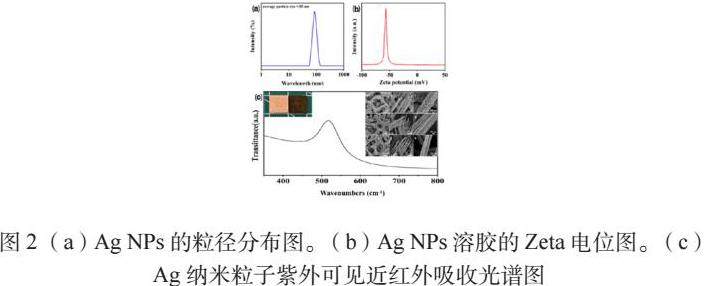
在现代纳米科技领域,粒径分布的精确测量对于合成纳米粒子的性能和应用至关重要。动态光散射(Dynamic Light Scattering,DLS)技术作为一种非侵入性的测量手段,因其能够提供纳米粒子粒径分布的详细信息而备受青睐。使用动态光散射粒度分析仪对合成的Ag NPs进行了粒径分布的测量,如图2(a)所示。结果显示Ag NPs的平均水合粒径约为85 nm,且主要集中在70 - 103 nm范围内。如图2(b)所示Zeta电位是描述胶体粒子在电场作用下迁移速度的参数,它与粒子表面的电荷状态密切相关。Ag NPs溶胶的Zeta电位为-57.8 mV,这一负值表明粒子表面吸附有带负电的柠檬酸根离子。柠檬酸是一种常用的稳定剂,能够通过其负电荷与Ag NPs表面相互作用,防止粒子聚集。Zeta电位的绝对值是评估胶体体系稳定性的重要指标。采用紫外可见近红外光谱仪对合成的Ag NPs观察粒径大小,如图2(c)所示,发现Ag NPs大小符合实验要求,从而进一步合成Au@Ag NPs,并展示了Au@Ag在泡沫铜上的有效附着。
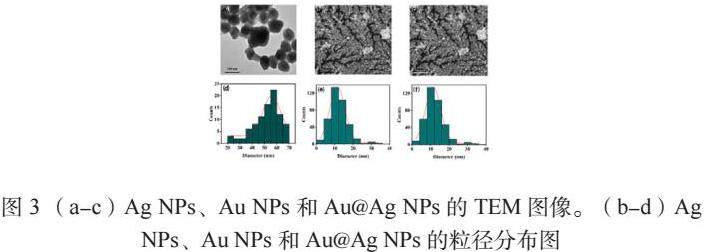
通过图3(a-c)所示的透射电子显微镜(Transmission Electron Microscopy,TEM)图像,能够直观清晰地观察到Ag NPs的微观形态,多为近似球形,且颗粒分散较为均匀。Au NPs呈现较为规则的球形形态,分布相对均匀。所合成的Au@Ag NPs呈现出较为规整的球形结构,且颗粒分散性良好。上述合成粒子彼此之间均没有明显的团聚现象。
图3(d-f)所示是AgNPs、Au NPs、Au@Ag NPs的粒径分布图,利用Lee-Meisel方法合成的Ag NPs平均粒径为50.1 ± 5.8 nm。这一结果不仅给出了合成所得AgNPs的平均粒径数据,同时其5.8的误差范围也体现了粒径存在一定的离散性。Au NPs的粒径分布较窄,粒径的峰值集中在15.21 nm附近,表明多数Au NPs的粒径接近该数值。Au@Ag NPs的粒径分布呈现出单峰特征,粒径的峰值出现在12.1 nm处,这表明在此粒径附近的Au@Ag NPs颗粒数量占比最高。上述说明了合成的纳米颗粒群体粒径相对集中,一致性较高。
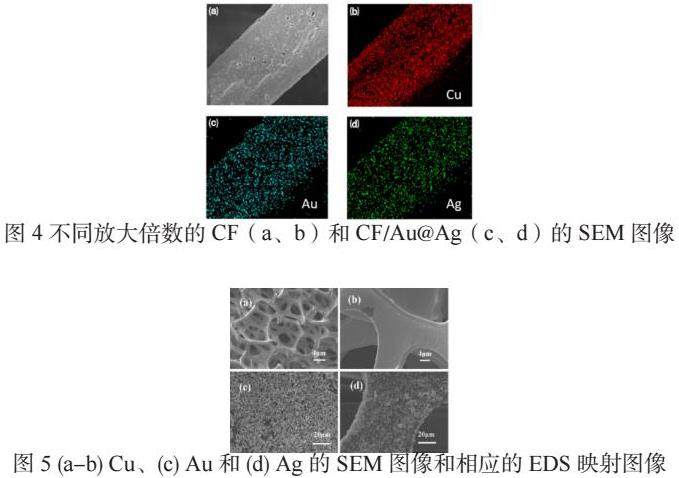
图4(a-b)为两种放大倍数的泡沫铜的扫描电子显微镜(Scanning Electron Microscopy,SEM)图像,清晰地显示了三维多孔、交联网格结构和光滑表面。CF具有多孔结构,大多为五边形,孔径范围为200 - 300 μm。图4(c-d)显示,物理沉积后Au@Ag纳米结构已在CF表面致密均匀地生长。如图5所示,SEM图像。Au和Ag元素均匀分布在泡沫铜上,表明Au@Ag纳米粒子在泡沫铜框架上附着完成。
介绍了一种基于泡沫铜的Au@Ag纳米溶液基底。取配制好不同浓度的标准肌酐与溶液。取适量混合溶液滴加到制备好的CF/Au@Ag基底上。使用拉曼光谱仪,在样品表面选取多个测量点进行测量,获取肌酐的特征拉曼信号。分析各条件下基底的SERS信号强度,确定最优条件。
3.2 肌酐的拉曼表征
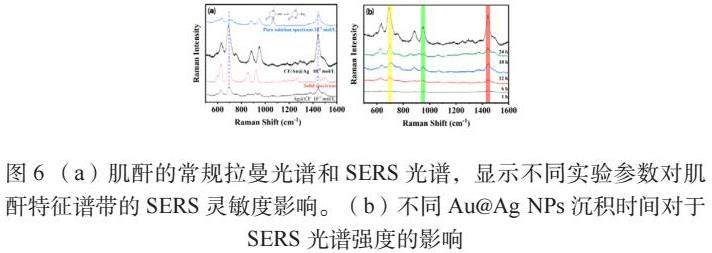
使用便携式拉曼光谱仪分别收集了粉末状固体和水性(10-3 mol L-1)肌酐的参考拉曼光谱。如图6(a)所示,固体样品在695 cm−1、925 cm−1和1438 cm−1处的特征拉曼光谱带在肌酐水溶液中分别移动到797 cm−1、947 cm−1和1446 cm−1。其他几个谱带也明显移动,表明肌酐分子环的结构在水溶液中发生了一定程度的变化。肌酐的SERS光谱与水性肌酐的拉曼光谱不同。然而,695 cm−1和925 cm−1处略微偏移的谱带表明存在肌酐。为了比较不同沉积时间对基底性能的影响,通过物理沉积制备了5种不同Au@Ag沉积时间的基底。通过特征峰强度筛选最佳沉积时间基底。如图6(b)所示,不同浸泡时间的基底的SERS光谱图可知,浸泡了24 h制备的CF/Au@Ag基底SERS信号最强。泡沫铜结构在干燥是表现一定的疏水性,Au@Ag纳米溶液不能有效均匀附着,通过长时间的浸泡有助于基底合成的均匀性,同时在一定浸泡时间后趋向于稳定。
3.3 CF/Au@Ag基底检测灵敏度优化
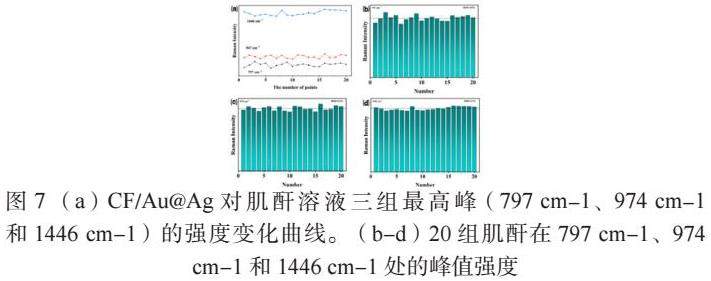
准确捕获目标分子、实现定量检测的基础首先依赖于构建合适的SERS基底。通常,SERS基底主要与纳米粒子的材质、形状、基底与分析物的亲和力以及纳米粒子之间的间隙有关。为了增加热点区域,选择80 nm Au@Ag作为SERS增强基底。采用Au@Ag修饰纳米粒子也能满足增强肌酐分子信号的要求,但遗憾的是表面Ag在空气中易被氧化失活,导致表面脏污、信号混乱,影响分析物目标峰的分辨率。本文提出一种配体修饰策略,用以减缓Ag的氧化速度从而更好地组装分子与纳米粒子。在CF/Au@Ag基底上随机选取20个点进行SERS检测,如图7(a-d)所示,在797 cm-1、974 cm-1和1446 cm-1三个位置的SERS信号均保持在相对平均的范围内,验证了CF/Au@Ag基底具有较优的均匀性。
3.4 肌酐水溶液的定量分析
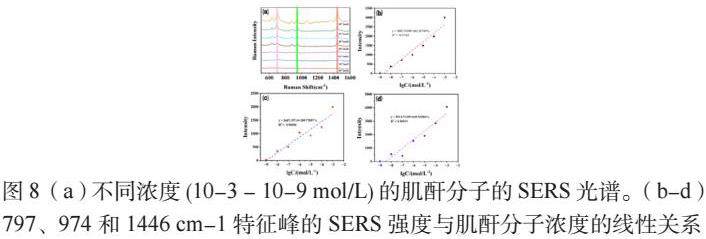
为了证明SERS基底可以定量检测分析物,在制备好的基底上方滴加不同浓度的肌酐混合溶液,浓度在0.5 mg·L−1以上即可清晰辨别出肌酐的特征峰,观察797 cm−1、974 cm-1和1446 cm-1处峰面积与浓度的关系。随着浓度的增加,SERS强度随之增加,如图8(a)所示,从而来定量分析尿液中的肌酐含量。
通过研究和分析它们之间的数量关系,并对数据进行对数线性拟合,得出了以下三个方程(797cm-1、974cm-1、1446cm-1特征峰线性系数方程分别用I797,I974,I1466表示)。
方程2.1、2.2、2.3所建立的线性关系将为精确评估尿液监测中的肌酐含量提供良好的理论支撑。
本实验中,基于对CF/Au@Ag基底性能的讨论,表现出优异的SERS性能,肌酐位于797 cm-1、974 cm-1和1446 cm-1处的特征峰被明确标识,这为临床诊断提供了丰富的“分子指纹”信息[15]。其中,797 cm-1处特征峰因为C—N拉伸;974 cm-1由于CH2的面外扭曲变形;位于1446 cm-1的特征峰是由于CH2的面外摇摆、CH3的面外摇摆以及面外扭曲变形引起的。随着肌酐浓度从10–3 mol/L下降到10–9 mol/L,这个特征峰的强度也相应减弱。因此,可以通过分析这三个特征峰的SERS强度与肌酐分子浓度对数之间的线性关系,来研究其变化规律。如图8(b-d)所示,三条拟合直线的线性系数0.9757、0.9611、0.9652。肌酐浓度检测可以达到10-8 mol/L依然相对清晰,因此,采用CF/Au@Ag作为SERS基底,通过低温处理可以显著增强肌酐分子的SERS活性。同时,SERS光谱显示出良好的线性关系,这为准确检测肌酐分子浓度提供了依据。这一发现有望在临床上应用于肌酐的定量检测,为评定肾脏功能提供更为快速的检测方法[16-18]。
4 讨论与结论
本研究制备的新型三维(3D)多孔功能泡沫金属表面增强拉曼散射基底(CF/Au@Ag),采用物理沉积策略在三维泡沫铜框架上附着金/银纳米粒子制成。通过三维空隙提高捕捉肌酐分子能力,促进了表面增强拉曼散射光谱活性。利用该基底对生理盐水中的肌酐进行无标记检测,在797 cm-1、974 cm-1和1446 cm-1特征峰处,SERS强度与肌酐分子浓度的线性相关系数R2分别达到0.9756、0.9610和0.9652。结果表明,CF/Au@Ag基底在常温下对肌酐浓度具有较高探测能力,灵敏度能够实现10-8 mol/L的精准检测。与之前cheng等人多采用的二维结构基底相比[19],不仅提高了对目标分子的捕捉能力,还显著提升了检测灵敏度(之前为10-6 mol/L)。采用SERS技术结合CF/Au@Ag纳米复合材料检测肌酐分子浓度,提高了检测的灵敏度和准确性,为临床提供了更可靠的检测方案,为快速尿液肌酐检测开辟了新方向,有助于提高临床诊断效率和患者护理质量。本研究的CF/Au@Ag 基底在检测肌酐方面取得了较好成果,下一步将继续深入研究。进一步优化CF/Au@Ag 基底的制备工艺,提高其稳定性和重现性。
综上所述,本研究的CF/Au@Ag基底在肌酐检测方面已取得良好效果,未来通过上述研究方向的深入探索有望进一步提升该技术在生物医学检测领域的应用价值,推动临床诊断技术的发展。
参考文献
1]MARTINEZ L,HE L.Detection of Mycotoxins in Food Using Surface-Enhanced Raman Spectroscopy: A Review [J].ACS applied bio materials,2021,4(1): 295-310.
[2]WU Y,YU W,YANG B,et al.Self-assembled two-dimensional gold nanoparticle film for sensitive nontargeted analysis of food additives with surface-enhanced Raman spectroscopy [J].Analyst,2018,143(10): 2363-8.
[3]SANTOS A O,VAZ A,RODRIGUES P,et al.Thin Films Sensor Devices for Mycotoxins Detection in Foods: Applications and Challenges [J].Chemosensors,2019,7(1).
[4]CHOU J-A,CHUNG C-L,HO P-C,et al.Organic Electrochemical Transistors/SERS-Active Hybrid Biosensors Featuring Gold Nanoparticles Immobilized on Thiol-Functionalized PEDOT Films [J].Frontiers in Chemistry,2019,7.
[5]LI S,LIU X,CHAI H,et al.Recent advances in the construction and analytical applications of metal-organic frameworks-based nanozymes [J].Trac-Trends in Analytical Chemistry,2018,105: 391-403.
[6]SARANGI N K,PRABHAKARAN A,ROANTREE M,et al.Evaluation of the passive permeability of antidepressants through pore-suspended lipid bilayer [J].Colloids and Surfaces B-Biointerfaces,2024,234.
[7]GIERLINGER N,SCHWANNINGER M.The potential of Raman microscopy and Raman imaging in plant research [J].Spectroscopy-an International Journal,2007,21(2): 69-89.
[8]TAO J,SANG D,ZHANG X,et al.An elevated urinary albumin-to-creatinine ratio increases the risk of incident cardia-cerebrovascular disease in individuals with type 2 diabetes [J].Diabetol Metab Syndr,2024,16(1): 30.
[9]STEFLEA R M,STROESCU R,GAFENCU M,et al.A Pilot Comparative Study between Creatinine- and Cystatin-C-Based Equations to Estimate GFR and Kidney Ultrasound Percentiles in Children with Congenital Anomalies of the Kidney and Urinary Tract [J].Diagnostics (Basel),2024,14(10).
[10]AVCI E,YILMAZ H,SAHINER N,et al.Label-Free Surface Enhanced Raman Spectroscopy for Cancer Detection [J].Cancers,2022,14(20).
[11]KUKKAR D,CHHILLAR M,KIM K-H.Application of SERS-based nanobiosensors to metabolite biomarkers of CKD [J].Biosensors & Bioelectronics,2023,232.
[12]WANG H,MALVADKAR N,KOYTEK S,et al.Quantitative analysis of creatinine in urine by metalized nanostructured parylene [J].Journal of Biomedical Optics,2010,15(2).
[13]LEE P C,MEISEL D.Adsorption and surface-enhanced Raman of dyes on silver and gold sols [J].The Journal of Physical Chemistry,1982,86(17): 3391-5.
[14]FRENS G.Controlled Nucleation for the Regulation of the Particle Size in Monodisperse Gold Suspensions [J].Nature Physical Science,1973,241(105): 20-2.
[15]TSENG Y-M,CHEN K-L,CHAO P-H,et al.Deep Learning-Assisted Surface-Enhanced Raman Scattering for Rapid Bacterial Identification [J].Acs Applied Materials & Interfaces,2023,15(22): 26398-406.
[16]韩萍萍,李玲,刘杰,等.肾脏深度对肾动态显像测定肾小球滤过率的影响 [J].中国医疗设备,2017,32(6): 66-9.
[17]何晶玲,林娴,龙春艳,等.超声造影评价兔失血性休克复苏早期肾血流灌注及与肾功能的相关性 [J].中国医疗设备,2022,37(4): 140-4.
[18]许晓岚,黄丙仓,张宏艳,等.时间-空间标记反转脉冲技术在慢性肾脏病分期中的初步研究 [J].中国医疗设备,2016,31(3): 70-3.
[19]SUN G,LI N,WANG D,et al.A Novel 3D Hierarchical Plasmonic Functional Cu@Co(3)O(4)@Ag Array as Intelligent SERS Sensing Platform with Trace Droplet Rapid Detection Ability for Pesticide Residue Detection on Fruits and Vegetables [J].Nanomaterials (Basel),2021,11(12).
基金项目:安徽省自然科学杰出青年科学基金项目(No.1808085J30)。
作者简介:魏柯君(1996.12)男,汉,安徽淮北,硕士研究生,安徽医科大学附属巢湖医院,物资设备科,职称:助理工程师,SERS在生物医学中的应用方向;通讯作者:薛长国,教授,纳米材料的制备及在环境和生物医疗的应用。





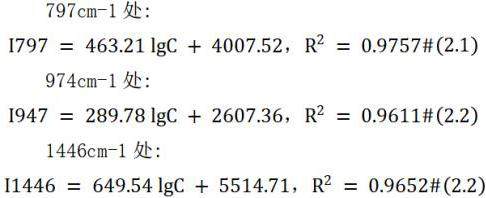

 京公网安备 11011302003690号
京公网安备 11011302003690号


