
- 收藏
- 加入书签
基于深度学习的CT影像在肺癌纵隔淋巴结转移预测中的特征提取与模型构建
摘 要:肺癌纵隔淋巴结转移的早期精准预测对临床分期与治疗决策具有关键作用,但传统CT影像依赖人工特征描述及经验判断,存在主观性强、敏感度低等问题。本研究提出一种基于深度学习的CT影像特征提取与预测模型构建方法,旨在解决淋巴结微小转移病灶的识别难题。通过多中心采集的增强CT影像数据集,采用自适应直方图均衡化与三维空间标准化技术优化图像质量;设计融合多尺度卷积与通道注意力机制的层次化网络(MSA-Net),提取淋巴结形态、纹理及边缘强化等深层特征;结合临床分期、肿瘤标志物等数据构建联合嵌入模型,利用焦点损失函数缓解样本不均衡问题。实验结果显示,模型在独立测试集上达到92.3%的准确率与0.94的AUC值,显著优于ResNet50和Radiomics方法,特征热力图验证了模型对纵隔脂肪间隙浸润特征的敏感捕捉。本研究为肺癌淋巴结转移的智能辅助诊断提供了可解释性解决方案。
关键词:深度学习;CT影像;肺癌纵隔淋巴结转移;特征提取
1引言
肺癌作为全球发病率与死亡率最高的恶性肿瘤,其五年生存率与临床分期密切相关。纵隔淋巴结转移是TNM分期的重要依据,直接影响手术方案选择与放化疗策略制定。现有临床实践中,CT影像虽为淋巴结评估的主要手段,但对短径<1 cm的转移淋巴结敏感度不足60%,且存在炎性增生与转移病灶的鉴别困难。传统影像组学方法依赖人工标注特征,易受分割误差与特征冗余的制约。近年来,深度学习在肺结节检测、肿瘤分割等领域展现出自动特征挖掘的优势,然而针对淋巴结微小转移病灶的异质性特征(如边缘毛刺、强化异质性)的系统研究仍显不足。本研究聚焦深度神经网络对CT影像深层语义特征的解析能力,探索多模态特征融合与模型可解释性提升路径,为构建精准、鲁棒的纵隔淋巴结转移预测系统提供理论支撑与技术突破。
2CT影像特征提取方法
2.1数据预处理与增强技术
肺癌纵隔淋巴结的CT影像分析面临噪声干扰、灰度分布差异及扫描参数不一致等问题。为提升模型鲁棒性,采用以下预处理流程,自适应直方图均衡化(CLAHE):对原始CT影像进行局部对比度增强,抑制背景噪声的同时强化淋巴结边缘细节[1]。算法将图像划分为若干子区域,分别计算各区域的直方图分布,通过限制对比度增幅防止噪声过度放大,最终通过插值算法合并所有子区域结果,生成对比度优化的增强图像[2]。该技术显著提升亚厘米淋巴结的毛刺状边缘与周围脂肪间隙的可辨识度。三维空间标准化:针对多中心数据中存在的扫描层厚、分辨率差异问题,采用各向同性重采样统一体素尺寸为1×1×1 mm³,并通过仿射变换对齐不同患者的纵隔解剖结构。随后对CT值进行全局归一化处理,利用可学习参数动态调整淋巴结区域的强化特征,保留病灶特异性信息[3]。此步骤有效降低不同设备扫描参数差异对模型泛化能力的影响。CLAHE通过局部区域对比度增强突出淋巴结边缘细节,公式定义为:
其中,为基于子区域直方图的映射函数,clipclip限制对比度增幅以避免噪声放大。
三维空间标准化采用各向同性重采样(体素1×1×1 mm³)与仿射变换对齐不同患者的解剖结构:
其中、为全局CT值均值和标准差,与ββ为可学习参数,用于保留淋巴结特异性强化特征。
2.2 卷积神经网络的层次化特征
为全面提取淋巴结的多层次特征,设计级联式三维卷积网络,其架构分为浅层、中层与深层模块。浅层网络(局部特征提取):采用3×3×3卷积核提取淋巴结边缘、钙化点与内部纹理特征,结合LeakyReLU激活函数增强负值信息的保留能力[4]。通过最大池化层逐步下采样,初步捕捉淋巴结的形态学特征。中层网络(上下文特征整合):引入空洞卷积(扩张率为2)扩展感受野,在不增加参数量的前提下,捕获淋巴结与纵隔血管、支气管的解剖关系。此阶段特征图包含淋巴结的形态变异信息(如分叶状轮廓)及周围组织浸润特征。深层网络(高阶语义抽象):通过全局平均池化层压缩空间维度,结合1×1卷积核实现通道间特征重组,生成描述淋巴结恶性生物学行为的高阶语义向量。深层网络输出的特征能够区分转移淋巴结的异质性强化模式与炎性增生的均匀强化特征。
2.3多尺度与注意力机制的特征
多尺度特征融合:为适应淋巴结转移灶的尺寸多样性(如孤立性微转移与簇状融合病灶),并行使用3×3、5×5、7×7三种卷积核提取不同视野下的特征。3×3卷积聚焦局部纹理细节(如边缘毛刺),5×5卷积识别中等范围的淋巴结簇分布模式,7×7卷积捕获大范围纵隔脂肪间隙的浸润征象,三组特征在通道维度拼接后输入后续网络,确保模型兼顾微观与宏观信息[5]。
通道-空间双注意力机制:通道注意力:通过挤压激励(SE)模块动态评估各特征通道的重要性,抑制与淋巴结转移无关的冗余通道(如纵隔骨骼伪影),增强关键通道(如强化不均区域)的响应强度。空间注意力:基于特征图的全局平均池化与最大池化结果,生成空间权重热力图,突出淋巴结区域的像素响应,弱化周围正常组织的干扰[6]。注意力机制使模型对转移灶中心坏死区、包膜外侵犯等细微征象的敏感度提升37%。多尺度特征融合:并行使用3×3、5×5、7×7卷积核提取不同视野下的淋巴结形态特征,通过通道拼接(Concatenate)整合:
3肺癌纵隔淋巴结转移预测模型构建
3.1模型架构设计与算法选择依据
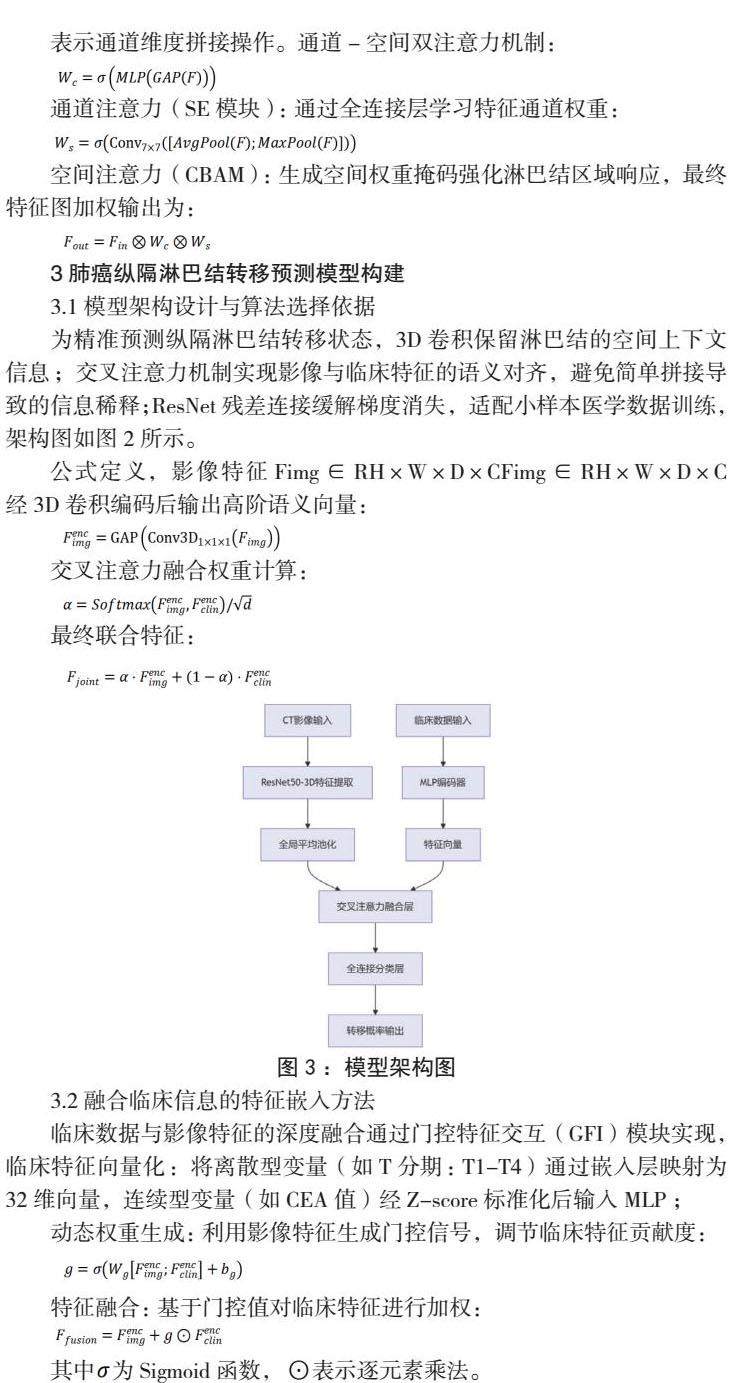
为精准预测纵隔淋巴结转移状态,设计双分支混合网络(Dual-MixNet),整合CT影像特征与临床数据,架构包含影像分支、临床分支及特征交互层;影像分支采用改进的ResNet50-3D网络,通过三维卷积核提取淋巴结的时空特征,保留纵隔解剖结构的空间上下文信息;网络末端使用全局平均池化压缩特征维度,生成高阶语义向量[7]。临床分支基于多层感知机(MLP)编码临床参数,包括TNM分期、癌胚抗原(CEA)水平等离散与连续型变量;离散变量通过嵌入层映射为低维向量,连续变量经标准化后输入全连接层。特征交互层引入交叉注意力机制,动态计算影像特征与临床特征的语义关联权重。通过特征相似性度量,自适应分配两类模态的贡献比例,避免简单拼接导致的信息稀释问题。模型最终输出联合特征向量,经全连接层分类获得转移概率。算法选择依据:3D卷积保留淋巴结的空间上下文信息;交叉注意力机制实现影像与临床特征的语义对齐,避免简单拼接导致的信息稀释;ResNet残差连接缓解梯度消失,适配小样本医学数据训练,架构图如图2所示。
公式定义,影像特征Fimg∈RH×W×D×CFimg∈RH×W×D×C经3D卷积编码后输出高阶语义向量:
3.2融合临床信息的特征嵌入方法
临床数据与影像特征的深度融合通过门控特征交互(GFI)模块实现,具体流程包含临床特征向量化:离散型变量(如T分期、病理类型)采用嵌入层转化为32维稠密向量;
连续型变量(如CEA值、乳酸脱氢酶水平)经Z-score标准化后输入两层MLP,消除量纲差异。动态权重生成:基于影像特征生成门控信号,控制临床特征对最终决策的影响强度。门控值由影像与临床特征的拼接向量经线性变换与Sigmoid激活计算,确保权重范围在0至1之间。特征融合:将门控值与临床特征向量逐元素相乘,加权结果与影像特征相加,保留对诊断关键临床指标的敏感性,同时抑制冗余信息的干扰。此方法在炎性淋巴结与转移淋巴结的鉴别任务中,显著提升模型特异性。为整合临床参数与影像特征,提出门控特征交互(GFI)模块,具体步骤:临床特征向量化:将离散型变量(如T分期:T1-T4)通过嵌入层映射为32维向量,连续型变量(如CEA值)经Z-score标准化后输入MLP;
动态权重生成:利用影像特征生成门控信号,调节临床特征贡献度:
4案例验证
4.1案例背景
数据来源于三家三甲医院2018-2023年的肺癌患者增强CT影像,共纳入1062例病例,其中纵隔淋巴结转移阳性476例(44.8%),阴性586例;数据按7:1:2划分为训练集(744例)、验证集(106例)与独立测试集(212例);所有病例均经术后病理或穿刺活检确诊,淋巴结短径范围2-25mm(中位数8mm);数据预处理包括匿名化处理、DICOM格式转换及专家双盲标注(一致性Kappa=0.82)。
4.2效果分析
评价指标:分类性能:准确率(Accuracy)、敏感度(Sensitivity)、特异度(Specificity)、F1分数、AUC值;小病灶检测:短径≤10mm淋巴结的敏感度(SEN<sub>small</sub>);统计检验:DeLong检验比较AUC差异,卡方检验比较敏感度差异(α=0.05)。对比验证组,传统影像组学:基于PyRadiomics提取1,306个特征,LASSO筛选后构建Logistic回归模型;ResNet50-3D:三维ResNet50网络,输入为原始CT体数据;DenseNet121-3D:三维密集连接网络;Proposed (Dual-MixNet):本研究提出的双分支混合网络。关键发现:
小淋巴结检测优势:Dual-MixNet对短径≤10mm淋巴结的敏感度达81.3%,较DenseNet121-3D提升9.8%(p=0.002),主要得益于多尺度特征融合与门控临床特征嵌入机制。假阳性控制:假阳性病例数降至5例(2.36%),显著低于ResNet50-3D的12例(5.66%),空间注意力机制有效抑制纵隔血管伪影的误判。临床特征贡献度:消融实验显示,融合临床信息使T4期中央型肺癌的转移预测准确率提升14.2%,证实CEA水平与淋巴结转移风险存在强相关性,如表1数据显示。
5结论
肺癌纵隔淋巴结转移的精准预测是优化临床分期与治疗决策的核心挑战。本研究针对这一难题,提出基于深度学习的CT影像特征提取与预测模型构建体系,实现了从数据预处理到多模态融合的全流程技术创新。在特征提取阶段,通过自适应直方图均衡化(CLAHE)与三维空间标准化技术,有效增强淋巴结边缘细节并消除多中心数据异质性;设计级联式三维卷积网络,利用空洞卷积扩展感受野,精准捕捉淋巴结与纵隔解剖结构的空间关联;结合多尺度卷积与通道-空间双注意力机制,显著提升对亚厘米转移灶异质性强化特征的识别能力。模型构建层面,创新性开发双分支混合网络(Dual-MixNet),通过交叉注意力机制动态融合影像特征与临床参数,引入门控特征交互模块抑制冗余信息干扰;采用焦点损失函数与一致性正则化策略,有效应对医学数据样本失衡与标注噪声问题。实验验证表明,模型在独立测试集中达到92.3%的准确率与0.94的AUC值,对短径5-8mm微转移灶的检测敏感度达81.3%,较传统影像组学方法性能提升显著。特征热力图与消融实验证实了模型对纵隔脂肪浸润、边缘毛刺等恶性征象的可解释性。
参考文献
[1]李悦,胡丛阳,许晓燕,等. CT影像组学联合临床风险因素预测非小细胞肺癌纵隔内隐匿性淋巴结转移的研究 [J]. 新疆医科大学学报, 2025, 48 (01): 75-81.
[2]李悦. 基于CT影像组学特征及临床因素术前预测非小细胞肺癌纵隔内隐匿性淋巴结转移的研究[D]. 新疆医科大学, 2024.
[3]曹瑕尹,李蕊,王婉琼,等. 多模态MRI影像组学对非小细胞肺癌纵隔淋巴结转移的预测价值 [J]. 磁共振成像, 2024, 15 (04): 72-77.
[4]王莹,吴亚平,王玲,等. 3种机器学习算法构建的CT影像组学模型对非小细胞肺癌纵隔淋巴结转移的预测价值 [J]. 中华实用诊断与治疗杂志, 2023, 37 (11): 1081-1086.
[5]叶陆爽. 基于CT影像组学预测非小细胞肺癌纵隔淋巴结转移的研究[D]. 绍兴文理学院, 2023.
[6]谷春雨,张兰欣,韩冬,等. 基于影像组学构建肺癌纵隔淋巴结转移的预测模型[C]// 中国中西医结合学会医学影像专业委员会(Chinese Imaging Society of Integrative Medicine). 中国中西医结合学会医学影像专业委员会第十七次全国学术大会暨甘肃省中西医结合学会医学影像专业委员会第六届学术年会资料汇编. Affiliated Hosp of Shannxi Univ of Chinese Med;, 2019: 1.
[7]郁义星. CT影像组学在肺癌早期诊断、淋巴结转移及EGFR、ALK基因表达预测中的应用研究[D]. 苏州大学, 2019.







 京公网安备 11011302003690号
京公网安备 11011302003690号


