
- 收藏
- 加入书签
云芝多糖对人食管鳞癌生物学特性的影响
摘 要:【目的】 应用云芝多糖作用食管鳞癌KYSE-30细胞,探讨其对食管鳞癌KYSE-30细胞生物学特性的影响。【方法】 通过Western blot检测云芝多糖孵育食管鳞癌细胞KYSE-30后,CXCR4蛋白表达的变化,通过Transwell法检测评估食管鳞癌细胞侵袭能力变化,MTT法检测评估食管鳞癌细胞KYSE-30与Matrigel 胶粘附能力的变化,划痕法检测评估食管鳞癌细胞KYSE-30迁移能力的变化。【结果】实验组KYSE-30细胞CXCR4 蛋白表达水平较空白组降低。云芝多糖孵育后,食管癌KYSE-30细胞粘附增强,侵袭及迁移能力下降。【结论】云芝多糖降低食管癌细胞CXCR4蛋白表达,可抑制食管癌KYSE-30细胞的转移潜能,提示云芝多糖可能可以通过CXCR4/CXCR4通路抑制食管鳞癌细胞转移特性。
关键词:食管癌;云芝多糖;CXCL12/CXCR4;转移
中图分类号:R734.1 文献标志码:A
Abstract:【Objective】The aim of this study was to explore the effects of Coriolus versicolor polysaccharide on the biological characteristics of esophageal squamous cell carcinoma KYSE-30 cells in vitro.【Methods】Western blot analysis was performed to detect changes in CXCR4 protein expression in esophageal squamous cell carcinoma cell line KYSE-30 following incubation with Coriolus versicolor polysaccharide. Changes in the invasive capacity of esophageal squamous cell carcinoma cells were assessed using the Transwell assay; alterations in the adhesive ability of cell line KYSE-30 to Matrigel matrix were evaluated via the MTT assay; and variations in the migratory capacity of cell line KYSE-30 were examined through the wound healing assay. 【Results】The CXCR4 protein expression level in the experimental group (cell line KYSE-30) was significantly lower than that in the control group. After incubation with Coriolus versicolor polysaccharide, KYSE-30 esophageal cancer cells exhibited enhanced cellular adhesion accompanied and a reduction in invasive capability and migratory capacity.【Conclusion】 Coriolus versicolor polysaccharide downregulates CXCR4 protein expression in esophageal cancer cells and effectively suppresses the metastatic potential of KYSE-30 cells. These findings suggest that Coriolus versicolor polysaccharide may inhibit the metastatic properties of esophageal squamous cell carcinoma by targeting the CXCR4/CXCR4 axis in cancer cells.
Key words:esophageal carcinoma;Coriolus versicolor polysaccharide;CXCL12/CXCR4 pathway;metastatic potential
食管癌在我国是较为常见的消化道恶性肿瘤之一,有着较高的发病率及死亡率,其中90%以上是食管鳞癌[1,2]。食管癌临床上往往发展迅速,易于转移。食管鳞癌细胞具有较强增殖、侵袭及转移能力,可侵犯食管粘膜下层、肌层、淋巴及血管进而侵犯食管周围组织并易于发生远处转移,导致手术根治困难及术后复发,是食管鳞癌治疗失败的重要原因之一。既往的研究显示肿瘤细胞的生物学行为与某些炎症反应有着相同的通路和机制,有学者研究[3,4]显示从药用菌类提取的多糖类物质可以通过对抗肿瘤及免疫调节等作用从而有效改善实体肿瘤患者的总体无病生存时间,同时还可以减少常规肿瘤治疗的副作用。本研究通过应用云芝多糖作用于食管鳞癌细胞KYSE-30,并观察云芝多糖对食管鳞癌细胞生物学特性的影响。
1.材料及方法
1.1 主要设备、细胞株与试剂
二氧化碳培养箱(SHELD-M2300,美国)、倒置显微镜(Olympus 日本)、DMSO(Sigma 美国)、96孔培养板(Corning 美国)、6孔培养板(Corning 美国)、FBS(杭州四季清公司 中国)、DMEM(Gibco美 国)、Transwell细胞培养小室(Corning 美国),Matrigel胶(BD 美国)、CXCR4一抗(abcam 美国)、云芝多糖(源叶生物 中国)。人食管鳞癌细胞株KYSE-30由中山大学肿瘤防治中心实验室提供。
1.2 细胞准备及培养
KYSE-30细胞在含DMEM的培养液(100ml/L胎牛血清)中,37℃、5%CO2、饱和湿度的条件下孵育箱中培养,待细胞培养至85%融合使用。
1.4 Western blot 检测CXCR4蛋白表达的变化
分实验组和空白组,实验组细胞使用含100μg/ml 云芝多糖的培养基培养,对照组细胞使用普通培养基培养,以相应培养液调节细胞悬液浓度,将调好细胞悬液以2ml/孔接种于6孔板,置于37℃、5%CO2饱和湿度条件下培养72h,使细胞充分贴壁生长。收集两组细胞进行总蛋白提取,分光光度计测蛋白浓度、定量,样品蛋白SDS-PAGE电泳分离,电转至PVDF膜上,配制适量5%脱脂牛奶封闭1小时,随后按照目的条带位置裁剪对应条带,并按照1∶1000的浓度配置足量一抗稀释液,CXCR4为目的条带,GAPDH为内参,4℃孵育过夜,第二天使用TBST缓冲液室温下洗3次,每次10min,加入对应二抗(1∶5000),室温下摇床孵育1h,放入TBST缓冲液室温下洗3次,每次10min,使用化学发光成像分析仪曝光,对曝光结果进行灰度扫描,计算CXCR4的相对表达量,CXCR4相对表达量=CXCR4灰度值/GAPDH 灰度值。
1.5 食管鳞癌KYSE-30细胞体外侵袭能力测定
实验分空白组及不同浓度实验组,不同浓度实验组细胞分别加入含50μg/ml、100μg/ml及200μg/ml云芝多糖培养液100μl,空白组细胞培养加入培养液100μl,以相应培养液调节细胞悬液浓度培养72h。在带有微孔的聚碳酸酯膜的Transwell小室上铺25μg Matrigel胶,取培养后48h的各组细胞消化,用培养液调成密度为5×104/ml的细胞悬液,每孔各取200μl加入上室,下室加入含DMEM(10%胎牛血清)细胞培养液在37℃、5%CO2和饱和湿度下共同孵育24h,每组设3平行样本,取出滤膜,用生理盐水清洗,擦净上室面细胞,40g/L多聚甲醛溶液固定30 min,吹干,0.1%结晶紫中染色30min,PBS液洗两遍,镜下观察。200倍光镜下随机选10个视野,计数滤过膜下室面细胞数。每孔设3个复孔,实验重复3次。
1.6 食管鳞癌 KYSE-30 细胞体外粘附能力测定
实验分空白组及实验组,实验组细胞加入200μg/ml云芝多糖培养液100μl,空白组细胞培养加入培养液100μl,以相应培养液调节细胞悬液浓度培养72h。无血清培养液稀释Matrigel胶至0.04mg/ml,96孔板至于冰上并每孔加入8μg已稀释的Matrigel胶,冷冻干燥,置 37℃、5%CO2孵育1h,加入10%胎牛血清200μl,包被备用。取各组细胞消化后,用细胞培养液调整各组细胞浓度为5×105/ml,每孔加入培养液200μl,摇床轻摇5 min,置于37℃、5%CO2孵育2h,弃细胞培养液,PBS液轻洗3次 ,每次轻摇3min,洗去各孔中未粘附的细胞,每孔加入0.4g/L MTT 100μl,轻摇5min,细胞培养箱培养4h,去MTT液,加入二甲亚砜200μl,轻摇,酶标仪检测(490nm)。设3个复孔,实验重复3次。粘附率=粘附细胞酶标仪检测值(490nm)/总细胞酶标仪检测值(490nm)。
1.7 食管鳞癌KYSE-30细胞体外迁移能力测定
实验分为实验组及空白组,不同浓度实验组细胞分别加入含100μg/ml及200μg/ml云芝多糖培养液100μl,空白组细胞培养加入培养液100μl,以相应培养液调节细胞悬液浓度,将调好细胞悬液以100μl/孔接种于六板孔中。37℃、5%CO2及饱和湿度下的条件培养,细胞长至90%时,弃原培养基,以100μl枪头划痕。PBS液清洗,去PBS液后即时快速拍照。不同组以相应培养液培养,每日拍摄照片。拍摄照片前吸出培养基,生理盐水清洗后拍摄,拍摄结束后将培养基移入6孔板。放置于37℃、5%CO2及饱和湿度下继续培养,观察不同组食管鳞癌细胞迁移爬满六孔板的时间。
1.8 统计学方法
Western blot所得相应的条带,采用图像分析软件进行扫描。计量资料x±s表示,应用SPSS10.0软件处理,样本均数间的比较采用T检验。
2 结 果
2.1云芝多糖对CXCR4蛋白的作用
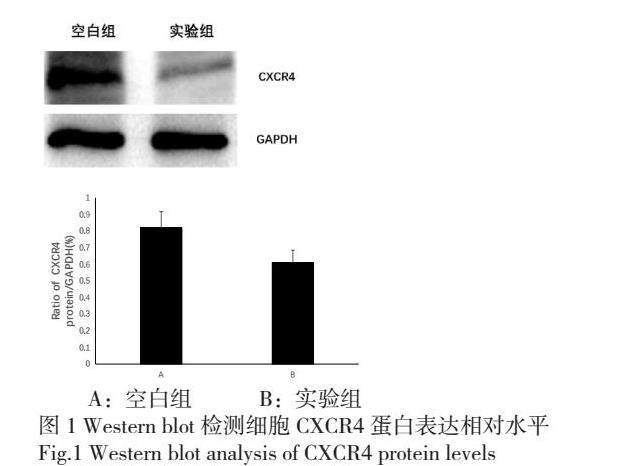
Western blot法检测空白组及实验组(100μg/ml云芝多糖作用72h)两组细胞CXCR4蛋白表达,灰度值测量三次。实验组CXCR4蛋白相对值为0.61±0.057,空白组0.82±0.097,差异明显(P < 0.05),见图 1。
2.2 食管鳞癌细胞侵袭能力的改变
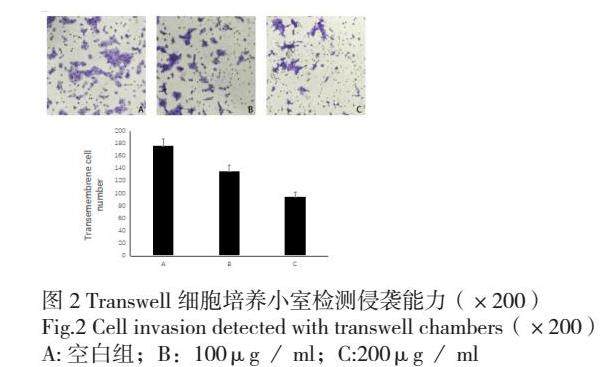
各组细胞培养72h后通过显微镜观察各组食管癌细胞穿过仿人基底膜的细胞数。200倍下10个视野,云芝多糖浓度为100μg/ml及200μg/ml 实 验 组 穿 膜细 胞 数 分 别 为 135.67±10.02及95.33±6.51,空白组为177.67±11.02。实验组侵袭能力较空白组减弱(P < 0.01),并随着培养液云芝多糖浓度上升,穿膜细胞数减少(图 2)。
2.3 食管鳞癌细胞粘附能力的改变
鳞癌细胞粘附实验,空白组细胞粘附率为(7.77±0.67)%,云芝多糖浓度200μg/ml实验组粘附率为(14.23±0.55)%,实验组粘附能力较空白组强(P < 0.05)。
2.4 食管鳞癌细胞迁移能力的改变
空白组及实验组,云芝多糖浓度为100μg/ml及 200μg/ml,观察各组24小时,48小时各组细胞迁移的结果:可见空白组48小时后已爬满6孔板,100μg/ml实验组迁移速度较空白组慢,200μg/ml组未见明显迁移(图 3)。

3 讨 论
食管鳞癌是较为常见的消化系统恶性肿瘤,大部分患者发现时已是中晚期,侵袭与转移是其重要的生物学特性。食管鳞癌细胞具有高侵袭及高转移特性,易于发生食管组织局部侵犯以及淋巴管、血管网发生远处转移。另有研究[5,6]表明炎症趋化因子通路深度参与多种肿瘤发展及转移等生物学行为,是导致肿瘤细胞发展、转移的重要一环,其中关于炎症趋化因子参与食管鳞癌发展的研究亦有报道[7]。
云芝是一种传统中药才,具有调节免疫力、抗肿瘤等多种药理学作用,与传统抗肿瘤药物相比基本没有明显的副作用。云芝多糖是云芝子实体通过脱脂、水提等多重工艺提纯的有效成份。研究[8-11]表明:云芝多糖往往通过多种不同的机制发挥抗肿瘤的作用,其中包括有效阻止肿瘤细胞由G1期进入S期,上调细胞周期调节蛋白p21(WAF/Cip1)和促凋亡蛋白Bax的表达进而诱导细胞的凋亡,在增强免疫细胞功能上也发挥重要作用,它可以增强γδT细胞和CD8+T 细胞抗肿瘤作用,同时,在一定浓度下,可以有效提高NK细胞的增殖率,明显促进其生长。我们既往的研究[12]显示:多糖类物质作为一种蛋白结合多糖,可以导致巨噬细胞表面的糖胺聚糖(glycosaminoglycans,GAGs)表达下调,从而影响炎症趋化因子表达,而云芝多糖是否可以通过相关机制影响食管鳞癌细胞炎症趋化因子通路,从而改变食管鳞癌细胞生物学特性,相关研究尚无明确结论。本研究通过云芝多糖作用于食管鳞癌细胞,观察CXCL12/CXCR4通路可能对食管鳞癌细胞生物学特性的影响。
侵袭与转移是食管鳞癌生物学行为重要特征。肿瘤细胞侵袭过程是肿瘤发展的重要阶段,当原发灶肿瘤细胞增殖到一定程度就会出现肿瘤细胞脱落并降解细胞外基质(ECM),从而进入脉管系统向远处转移,既往的研究[13,14]提示在肿瘤的发生、发展过程中趋化因子CXCL12/CXCR4轴扮演了重要的角色。CXCL12是基质细胞衍生因子(steomal cell derived factor-1,SDF-1),CXCR4是CXCL12的主要受体。Shen[15]等人发现:CXCL12/CXCR4轴在促进胰腺癌细胞的增殖与侵袭过程中起到了重要的作用。Daisuke[16]研究显示:CXCL12通过增强胃癌细胞中整合素β1的聚集促进胃癌细胞侵袭作用,导致胃癌进展,抑制CXCL12/CXCR4轴的信号传导通路可能是胃癌治疗的有效策略。本研究中使用不同浓度的云芝多糖培养液孵育食管鳞癌细胞后,培养组穿过Transwell细胞培养小室仿人基底膜的食管鳞癌细胞数显著少于空白组,并且随着培养液云芝多糖浓度升高,其穿膜细胞数呈现下降趋势,显示云芝多糖可能可以抑制食管鳞癌细胞侵袭能力。迁移是肿瘤细胞另外一种重要能力。Wang[17]等人的研究发现:CXCL12/CXCR4通过ERK/Ets-1途径可上调整合素αvβ6,从而诱导结直肠癌细胞定向迁移,研究[18]显示食管癌干细胞不仅自分泌大量CXCL12,而且其相应受体CXCR4也高表达,CXCL12/CXCR4可激活ERK1/2通路,从而最终维持食管癌干细胞高水平侵袭和转移的特征。本实验中,云芝多糖培养液孵育食管鳞癌细胞后,培养组食管鳞癌细胞迁移速度明显减慢,且培养液浓度越高,迁移速度越慢,提示云芝多糖可以一定程度抑制食管鳞癌细胞的迁移特性。肿瘤细胞与细胞外基质(ECM)的粘附是很重要一环,肿瘤局部发展,粘附作用很关键,肿瘤转移过程中,两者间解粘附作用可协助肿瘤细胞完成从原发灶脱离并侵入及破坏基底膜的过程,基底膜粘附作用下降可协助肿瘤细胞完成从原发灶脱离并侵入及破坏基底膜的过程,Dinesh等[19]的研究显示,乳腺癌细胞可促使肿瘤相关成纤维细胞分泌CXCL12,通过降低了内皮细胞的紧密连接,并下调了粘附连接蛋白的表达,从而导致血管通透性增加,使肿瘤细胞浸润增加。本研究中实验组鳞癌细胞粘附作用较空白组增强,提示云芝多糖可能可以增加食管鳞癌细胞粘附能力,减弱其转移特性。
CXCL12作为CXC类趋化因子,CXCR4是其主要的受体,云芝多糖孵育后,CXCR4的蛋白表达减弱,鳞癌细胞侵袭、迁移特性受到抑制。我们分析云芝多糖可以一定程度上抑制CXCL12/CXCR4轴受体CXCR4的表达,从而有效降低其特异性配体CXCL12的生物学效应,降低鳞癌细胞的转移特性。综上所述,云芝多糖可以通过炎症通路抑制食管鳞癌细胞发展转移能力,结合其无明显毒副作用,可能可以成为食管鳞癌治疗新的切入点。
参 考 文 献
[1] Sung H,Ferlay J,Siegel RL,et al. Global Cancer Statistics 2020: GLOBOCAN Estimates of Incidence and Mortality Worldwide for 36 Cancers in 185 Countries[J]. CA Cancer J Clin.CA Cancer J Clin,2021,71(3):209-24.
[2] Abnet CC, Arnold M, Wei WQ. Epidemiology of Esophageal Squamous Cell Carcinoma[J].Gastroenterology 2018,154 (2): 360–73.
[3] Wasser SP. Medicinal mushrooms as a source of antitumor and immunomodulating polysaccharides [J]. Appl Microbiol Biotechnol,2002,60(3):258-274.
[4] Jeitler M, Michalsen A, Frings D,et al. Significance of Medicinal Mushrooms in Integrative Oncology: A Narrative Review[J]. Front Pharmacol. 2020,11;11: 580656.
[5] Ieranò C, D'Alterio C, Giarra S, et, al. CXCL12 loaded-dermal filler captures CXCR4 expressing melanoma circulating tumor cells[J]. Cell Death Dis. 2019,10(8):562.
[6] Lu G, Qiu Y, Su X. Targeting CXCL12-CXCR4 Signaling Enhances Immune Checkpoint Blockade Therapy Against Triple Negative Breast Cancer[J]. Eur J Pharm Sci.2021,1;157:105606.
[7] Wang X, Cao Y, Zhang S, et,al. Stem cell autocrine CXCL12/CXCR4 stimulates invasion and metastasis of esophageal cancer [J]. Oncotarget. 2017,8(22):36149-36160.
[8] Onishi H, Morisaki T, Nakao F, et,al.Protein-bound polysaccharide decreases invasiveness and proliferation in pancreatic cancer by inhibition of hedgehog signaling and HIF-1α pathways under hypoxia[J].Cancer Lett.2013,335 (2):289-98.
[9] Rosendahl AH, Sun C, Wu D, et,al. Polysaccharide-K (PSK) increases p21(WAF/Cip1) and promotes apoptosis in pancreatic cancer cells. Pancreatology[J]. 2012,12(6):467-74.
[10] 孙飞,陶正中,周忠海等,云芝多糖增强人 NK 细胞杀伤功能的体外研究 [J].《生物医学工程与临床》. 2017, 21(2):126-131.
[11] Inatsuka C, Yang Y, Gad E, et,al. Gamma delta T cells are activated by polysaccharide K(PSK) and contribute to the anti-tumor effect of PSK[J]. Cancer Immunol Immunother. 2013;62(8):1335-45.
[12] Lou N, Ma G, Wang DF, et al. Effect of Coriolus
versicolor polysaccharide B on membrane glycosaminoglycans and cellular glutathione changes in RAW264.7 macrophages exposed to angiotensin Ⅱ[J].J South Med Univ,2007,27(12):1824-1826.
[13] Lu G, Qiu Y, Su X. Targeting CXCL12-CXCR4 Signaling Enhances Immune Checkpoint Blockade Therapy Against Triple Negative Breast Cancer[J]. Eur J Pharm Sci,2020,15(7):105606-105612.
[14] Ieranò C, D'Alterio C, Giarra S, et,al. CXCL12 loaded-dermal filler captures CXCR4 expressing melanoma circulating tumor cells[J]. Cell Death Dis. 2019,10(8):562-571.
[15] Shen B,Zheng MQ,Lu JW,et,al.CXCL12-CXCR4 promotes proliferation and invasion of pancreatic cancer cells[J]. Asian Pac J Cancer Prev.2013;14(9):5403-8.
[16] Izumi D,Ishimoto T, Miyake K,et,al.CXCL12/CXCR4 activation by cancer-associated fibroblasts promotes integrin β1 clustering and invasiveness in gastric cancer[J]. Int J Cancer.2016;138(5):1207-19.
[17] Wang B, Wang W, Niu W,et,al. SDF-1/CXCR4 axis promotes directional migration of colorectal cancer cells through upregulation of integrin αvβ6[J]. Carcinogenesis.2014; 35(2): 282-91.
[18] Wang X, Cao Y, Zhang S, et,al. Stem cell autocrine CXCL12/CXCR4 stimulates invasion and metastasis of esophageal cancer[J]. Oncotarget. 2017;8(22):36149-36160.
[19] Ahirwar DK, Nasser MW, Ouseph MM, et,al. Fibroblast-derived CXCL12 promotes breast cancer metastasis by facilitating tumor cell intravasation[J]. Oncogene. 2018, (32):4428-4442.
基金项目:广东省中医药局科研项目(20231062),广东省中医药局科研项目(20221082),广东省食管癌研究所科技计划项目(M202211)
通讯作者:戎煜明E-mail:rongym@sysucc.org.cn 汪道峰 E-mail:wangdf@sysucc.org.cn






 京公网安备 11011302003690号
京公网安备 11011302003690号


