
- 收藏
- 加入书签
冬虫夏草子实体7个单体化合物体外抗肝纤维化研究
摘要:目的:探究冬虫夏草(Ophiocordycepssinensis)子实体有效成分 7 个单体化合物抗肝纤维化效果。方法:利用转化生长因子(TGF-β1)诱导肝星状细胞(LX-2)构建肝纤维化模型,通过 CCK8 法检测不同浓度化合物对 LX-2 细胞的活性,同时设立正常组(无处理)、模型组(TGF-β1 10.0 ng/mL)、阳性组(复方鳖甲软肝片 75.0 ng/mL + TGF-β1 10. 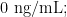 )、化合物组(活性浓度+TGF-β1 10.0 ng/mL),应用实时荧光定量(qPCR)和蛋白免疫印迹(WB)检测这些化合物组对TGF-β1 诱导LX-2 细胞中基因mRNA 和相关蛋白相对表达量的影响。结果:7 个单体化合物和阳性药物组浓度分别为7.5 μM、10.0 μM、10.0 μM、10.0 μM、5.0 μM、50.0 μM、25.0 μM、75.0ng/mL 时对 TGF-β1 诱导 LX-2 细胞活性均较低;通过 qPCR 法测定 TGF-β1 诱导的 LX-2 细胞纤维化相关基因的 mRNA 表达,与对照组相比,发现啤酒甾醇组中 Samd3、Smad4、Collagen I 的 mRNA 相对表达量显著下调 (P<θ, .01);通过 Western blot 测定TGF-β1 诱导的LX-2 细胞表达纤维化相关蛋白,与对照组相比,发现啤酒甾醇组中Smad3、Smad4 蛋白相对表达量显著下调 (P<θ? .01)。结论:冬虫夏草子实体单体化合物啤酒甾醇显著抑制 TGF-β1 诱导的 LX2 细胞纤维化相关基因和蛋白的表达,表明啤酒甾醇具有抗纤维化作用,但作用效果不及复方鳖甲软肝片。其肝纤维化机制可能与抑制TGF-β 诱导的LX-2 细胞的异常活化和增殖,通过调节TGF-β/Smads 中关键基因Samd3、Smad4 的转录和表达,使肝组织中Collagen I 蛋白沉积或降解有关。本研究旨在为冬虫夏草资源有效开发利用提供科学依据。
)、化合物组(活性浓度+TGF-β1 10.0 ng/mL),应用实时荧光定量(qPCR)和蛋白免疫印迹(WB)检测这些化合物组对TGF-β1 诱导LX-2 细胞中基因mRNA 和相关蛋白相对表达量的影响。结果:7 个单体化合物和阳性药物组浓度分别为7.5 μM、10.0 μM、10.0 μM、10.0 μM、5.0 μM、50.0 μM、25.0 μM、75.0ng/mL 时对 TGF-β1 诱导 LX-2 细胞活性均较低;通过 qPCR 法测定 TGF-β1 诱导的 LX-2 细胞纤维化相关基因的 mRNA 表达,与对照组相比,发现啤酒甾醇组中 Samd3、Smad4、Collagen I 的 mRNA 相对表达量显著下调 (P<θ, .01);通过 Western blot 测定TGF-β1 诱导的LX-2 细胞表达纤维化相关蛋白,与对照组相比,发现啤酒甾醇组中Smad3、Smad4 蛋白相对表达量显著下调 (P<θ? .01)。结论:冬虫夏草子实体单体化合物啤酒甾醇显著抑制 TGF-β1 诱导的 LX2 细胞纤维化相关基因和蛋白的表达,表明啤酒甾醇具有抗纤维化作用,但作用效果不及复方鳖甲软肝片。其肝纤维化机制可能与抑制TGF-β 诱导的LX-2 细胞的异常活化和增殖,通过调节TGF-β/Smads 中关键基因Samd3、Smad4 的转录和表达,使肝组织中Collagen I 蛋白沉积或降解有关。本研究旨在为冬虫夏草资源有效开发利用提供科学依据。
关键词:纤维化;LX-2;单体化合物;TGF-β1/Smad
中图分类号 Q71 文献标识码 A
冬虫夏草(ChineseCordyceps)属于麦角菌科(Clavicipitaceae)虫草属(Cordyceps),为该真菌寄生于鳞翅目(Lepidoptera)蝙蝠蛾科(Hepialidae)昆虫幼虫体内后形成的复合体[1]。冬虫夏草是一味传统名贵中药材,具有特殊的药用价值以及食用价值[2]。冬虫夏草的入药部位为菌核(寄主体内菌丝)和子座的复合体,具有特殊的腥气,味甘,性温[4-5],其粉末呈棕色[3]。在藏医学典籍《月王药诊》、《藏本草》、《图鉴》及《金汁甘露宝瓶札记》中,冬虫夏草被认为具有治疗肺部疾病的功效[1]。现代研究表明[6],冬虫夏草的主要化学成分为八大类,包括氨基酸类、环肽类、核苷类、甾醇类、多糖类、有机酸类、维生素类和微量元素。其中甾醇类化合物是冬虫夏草药理作用的重要组成部分。研究表明,甾醇类化合物具有显著的抗炎[7]、抗氧化性能[8]、增强机体免疫力[9]、抑制肿瘤细胞的分化[10]等作用。
肝纤维化(HF)为各种慢性肝病的共同病理过 是慢性肝炎发展至肝硬化的必经阶段[11]。肝纤维化的初始损伤通常由病毒性肝炎(如乙 身免疫性疾病或其他慢性肝损伤因素引起[12-13]。在慢性炎症状态下 合成和分泌胶原蛋白和其他细胞外基质成分, j*e 生的活性氧 脏的代谢、解毒等功能,导致肝功能障碍,促进肝纤维化的发 ,冬虫夏草具有一定的抗纤维化作用[18-21]但目前冬虫夏草何种活性成分在治疗肝纤维化时发挥疗效的研究未见报道。
为了深入研究冬虫夏草的活性成分,有效利用其珍稀资源,本研究在前期进行了冬虫夏草子实体单体化合物的分离鉴定,得到了 7 个单体化合物;在此基础上,利用转化生长因子(TGF-β1)诱导肝星状细胞(LX-2)构建肝纤维化模型,对冬虫夏草子实体中 7 个单体化合物进行体外抗肝纤维化评价,从而为有效开发利用冬虫夏草提供实验依据。
1 材料与方法
1.1 实验材料
人肝星形细胞LX-2(CL-0560)由武汉普诺赛生命科技有限公司提供;单体化合物为课题组前期分离鉴定所得,分别为化合物腺苷(Adenosine)、尿苷(Uridine)、麦角甾醇(Er rol)、啤酒甾醇(Cerevisterol)、L- 色 氨 酸 ( L-Tryptophan ) 、 2- 哌 啶 酮 ( 2-Piperidinone ) 、 甾 体 衍 生 物[(4S)-ergost-((8)-en-3β,5α,6β-triol)]。
1.2 仪器与试剂耗材
1.2.1 仪器
Western blot 电泳仪(DYY-6C)(北京六一生物科技有限公司);化学发光成像系统(广州誉维生物科技仪器有限公司);温控系统 BCD-216F TB 4 ℃冰箱(青岛海尔股份有限公司);超声波细胞粉碎机(宁波新芝生物科技股份有限公司);SIM-F140ADL 制冰机(松下电器产业株式会社);孵育盒(个/Pcs);电热恒温培养箱(上海跃进医疗器械有限公司)。
1.2.2 试剂耗材
DMEM 高糖培养基(赛默飞世尔科技)、胎牛血清(赛默飞世尔科技)、双抗(赛默飞世尔科技)、PBS(赛默飞世尔科技)、0.25 %胰蛋白酶(赛默飞世尔科技)、TGF-β1(百普赛斯)、CCK8 胞增殖-毒性检测试剂盒(北京兰杰柯科技有限公司)、抗体 SMAD3 Monoclonal antibody、抗体 SMAD4 Polyclonal antibody、抗体 Anti betaactin antibody(广州创伟生物有限公司)、无水乙醇(批号:20220501)、甲醇(批号:20220501)、异丙醇(批号:20220501)等购自上海创赛科技有限公司、水为 Millipore 超纯水。
1.3 实验方法
1.3.1 基本溶液配置
500.0 L MEM 培养基中加入 56.2 L 胎牛血清和 5.6 L 双抗混匀,配置成完全培养基,分装,备用;1 00mL 双蒸水中加入 PBS 标准品 0.2 g 氯化钾、8.0 g 氯化钠、0.2 g 磷酸二氢钾、1.4 g 磷酸氢二钠,PH 值调为7.4,配置成 PBS 缓冲液,250.0 mL 玻璃瓶分装,灭菌,备用;500.0 μL 双蒸水中加入 50.0 μg TGF-β1 蛋白粉末溶解为 100.0 μg/mL 的 TGF-β1 溶液混匀,配置成 TGF-β1 溶液。
1.3.2 细胞培养
LX-2 细胞复苏(液氮取出,37 ℃解冻后,1 200 rpm 离心3 min,DMEM 重悬培养);传代(吸出原培养液,PBS 清洗后0.25 %胰酶消化,加入含血清的培养基终止消化,按比例1:2 或1:3 接种接种);液氮冻存。
1.3.3 肝纤维化模型构建
在96 孔板中接种细胞悬液,同时设空白组和正常组,LX-2 细胞(1³10⁴/mL)经不同浓度TGF-β1 处理24-168h 后,利用CCK8 法法测定吸光度,重复3 次,取平均值,计算细胞活力,筛选TGF-β1 诱导 LX-2 细胞的最佳浓度建模;调整细胞浓度至 1×10∘/mL ,分为正常组和模型组,模型组中加入 10.0 ng/mL TGF-β1 观察,和空白组对比,细胞形态变化为纺锤体形状时模型建成时间[22]。
1.3.4 不同浓度化合物对LX-2 细胞活性的影响
LX-2 细胞( .1×10∘ /mL)接种于96 孔板,培养4 h 后贴壁,弃去上清液,PBS 缓冲液冲洗。再加入含不同浓度的单体化合物和复方鳖甲软肝片的培养基,培养24 h,加入CCK8(6 次重复),计算抑制率。
1.3.5 化合物对肝纤维化模型干预的LX-2 细胞活性的影响
LX-2 细胞 (2.5×104/mL) )接种于96 孔板,每孔加入200 μL 的DMEM 完全培养液,培养24 h 后弃去培养液。同时设立空白组、模型组、阳性组、化合物组。每孔体积为200.0 μL,恒温培养120 h 后,将模型组培养液全部弃去,加入最适活性浓度7 个单体化合物和复方鳖甲软肝片,培养48 h,CCK8 法(6 次重复)计算抑制率。
1.3.6 实时荧光定量 PCR
倒出培养基后用PBS 缓冲液清洗,加入 2.5 mL Trizol 试剂摇晃,用枪吹打使细胞裂解,转移到离心管,再用枪吹打至裂解液中无沉淀,冷藏静置15 min;向裂解液加入500.0 μL 氯仿,振荡30 s,溶液呈现乳浊状后冷藏静置 15 min,离心至样品分为 3 层,将上层水相转移至离心管中;加入异丙醇混匀,冷藏静置 10 min,离心后去上清液,加入 1.0 mL 75 %乙醇洗涤沉淀,再离心弃去上清,重复三次;晾干,加入 RNase-free 水溶解沉淀,待沉淀溶解后置于-80 ℃保存。引物见表1(生工生物工程上海股份有限公司),反应条件:37 ℃,温育2 min;55 ℃,温育15 min;85 ℃,孵育5 min,终止反应,将获得的产物-20 ℃保存。
表1 引物序列

1.3.7 蛋白免疫印迹 WB溶解RIPA 裂解液,混匀后倒去培养液,用PBS 缓冲液清洗,加入500 μL 裂解液,用移液器枪吹打,冰上裂解 10min ;根据样品数量,配制 BCA 工作液;2.0 mg 的蛋白标准中加入 1.0 mL 蛋白标准配制液充分溶解后稀释;将待测蛋白、不同浓度标准品加到96 孔板中;向各孔加入200.0 μL BCA 工作液,孵育30 min,酶标仪测定562 nm 波长处吸光度。
取 2 700.0 μL 下层胶预混液( (2×) )和下层胶缓冲液 (2×) 混匀,向上述混合液加入60.0 μL 改良型凝胶催化剂混匀;将上述混合液注入大制胶玻璃板中,加入异丙醇覆盖于下层胶之上,待下层胶凝固后后倒去异丙醇;取750.0 μL 上层胶预混液 (2×) )和上层胶缓冲液(2³)混匀,向上一步的混合液中加入15.0 μL 的凝胶催化剂混匀,将混合液注入制胶玻璃板中,插入梳齿,待上层胶凝固后,拔去梳齿;用微量移液枪向凝胶孔中依次加入样品和蛋白Marker 各 20.0 μL、5.0 μL;将胶架放入电泳槽中(电压120V,时间 90min; );取快速转膜液 100.0 L,加入去离子水和甲醇各 500.0 L、100.0 L,搅拌均匀并容至 1.0 得到 1× 工作液(电泳 400 mA,时间30 min);完成转膜后,在容器中加入 Western 快速封闭液完全没过膜,封闭 10 min;在孵育盒中加入一抗,将膜放入孵育盒,摇床上过夜(2 h, 4‰ );取出膜,用 TBST 洗涤后室温孵育二抗 1.5 h,再次用TBST 洗涤;按体积比例1:1 将超敏ECL 化学发光检测试剂盒A 液和B 液混合;从TBST 缓冲液中取出膜,吸去膜上缓冲液,将膜上有蛋白的面铺在工作台上,加上工作稀释液,孵育2 min,显影拍摄。
1.5 数据处理
数据分析和统计图分别用 SPSS 22.0 和 GraphPad Prism 8.0.2 软件完成;组间差异比较采用单因素方差分析, p< 0. 05为差异有统计学意义。
2 结果与分析
2.1 筛选TGF-β1 诱导 LX-2 细胞建模的最佳浓度和时间
在不同浓度作用下,细胞增殖率随时间的变化见图1。当作用时间延长至72 h 时, 10.0ng/mL TGF-β1 处理组OD450 值显著升高,增殖率达峰值, 24 h 组比较具有显著性差异(* P<0.01)。虽然高浓度组20.0 g/mL和 40.0 ng/mL 早期 24 效应, 随处 间延长细胞活力出现增殖抑制,尤其当作用时间达 120 h 时,各组细 程度下降。 诱导 72 后细胞的形态学变化见图 2,与正常组相比,模型组细胞经诱导72 HH 生变化。 售今 定 .0 ng/mL 和 72 h 为建立 TGF-β1诱导LX-2 细胞肝纤维化模型的最佳浓度和时间。
图1 不同浓度和不同时间的TGF-β1 对LX-2 细胞活力的影响
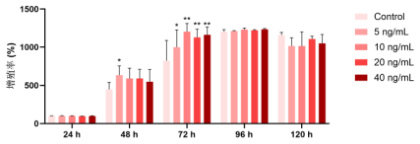
注:与 24 h 同浓度比较(*P <θ. .01)
图2 正常组与模型组TGF-β1 诱导72 h 后LX-2 细胞的形态学变化
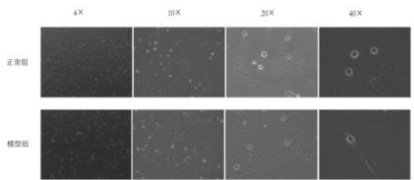
2.2 不同浓度化合物对LX-2 细胞活性的影响
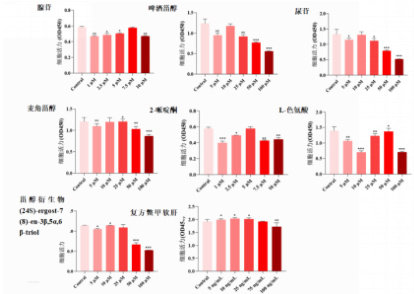
24 h 后不同浓度的腺苷、啤酒甾醇、尿苷、麦角甾醇、2- 哌啶酮、L- 色氨酸、甾醇衍生物[(4S)-ergost-((8)-en-3β,5α,6β-triol)]、复方鳖甲软肝片对 LX-2 细胞增殖活力的影响见图 3。单体化合物啤酒甾醇、尿苷、麦角甾醇、L-色氨酸、甾体衍生[(4S)-ergost-((8)-en-3β,5α,6β-triol)]浓度在 5.0 μM、10.0 μM、25.0 μM、50.0 μM、100.0 μM 下和单体化合物腺苷、2-哌啶酮浓度在 1.0 μM、2.5 μM、5.0 μM、7.5 μM、10.0 μM 下毒性均较低。与对照组相比,腺苷浓度在7.5 μM 时对LX-2 细胞活力影响小;啤酒甾醇在浓度在 10.0 μM 时对LX-2 细胞活力影响小;尿苷浓度在 10.0 μM 时对 LX-2 细胞活力影响小;麦角甾醇在浓度在10.0 μM 时对LX-2 细胞活力影响小;2-哌啶酮浓度在5.0 μM 时对LX-2 细胞活力影响小;L-色氨酸浓度在 50.0 μM 对 LX-2 细胞活力影响小;甾醇衍生物甾醇衍生物[(4S)-ergost-((8)-en-3β,5α,6β-triol)]浓度在 25.0 μM 时对LX-2 细胞活力影响小;阳性对照复方鳖甲软肝片浓度75.0 ng/mL 时在对LX-2 细胞活力影响较小。故后续体外实验腺苷、啤酒甾醇、尿苷、麦角甾醇、2-哌啶酮、L- 色氨酸、甾醇衍生物[(4S)-ergost-((8)-en-3β,5α,6β-triol)]、复方鳖甲软肝片的浓度分别为 7.5 μM、10.0 μM、10.0 μM、10.0 μM、5.0 μM、50.0 μM、25.0 μM、75.0 ng/mL 作为细胞活性研究。
图3 不同化合物对LX-2 细胞活力的影响
2.3 化合物对TGF-β1 诱导的肝纤维化模型细胞的影响
LX-2 细胞接种在96 孔板贴壁4 h 后分为10 组,分别为为:正常组(无处理)、模型组(TGF-β1 10.0 ng/mL)、阳性组(复方鳖甲软肝片 75.0 ng/mL + TGF-β1 10.0 ng/mL)及 7 个化合物处理组(含相应活性浓度+TGF-β110.0ng/mL) )。各组LX-2 细胞活力呈时间增长见图4,LX-2 细胞活力72 h 相较于24 h 和48 h 时显著增强,在96 h 时LX-2 细胞活力达峰值。此时,与正常组相比,阳性组、腺苷组和啤酒甾醇组 LX-2 细胞活力均呈现显著性差异( *P<0. .05)。因此,将以阳性组复方鳖甲软肝片、腺苷、啤酒甾醇进行后续体外实验。
图4 不同化合物对TGF-β1 诱导的LX-2 细胞活力的影响

2.4 实时荧光定量 PCR
LX-2 细胞中 Smad3、Smad4 及 Collagen I mRNA 相对表达量见图 5。相较于对照组,模型组(TGF-β1 10.0ng/mL) )、阳性组(复方鳖甲软肝片 75.0ng/mL+ GF-β1 0.0 g/mL)、腺苷组(7.5 μM+ GF-β1 0.0 g/mL)和啤酒甾醇组(10.0 μM+ TGF-β1 10.0 ng/mL)的 Smad3、Smad4 及 Collagen I mRNA 基因表达量均呈上升趋势,其中模型组中Smad3、Smad4 及Collagen I 基因 mRNA 相对表达量均显著上调。与模型组相比,阳性组、腺苷组和啤酒甾醇组基因表达量水平均降低,其中啤酒甾醇组的Smad3、Smad4 及Collagen I 基因 mRNA 相对表达量显著下调(#P <0.05) )。说明阳性组、腺苷组和啤酒甾醇组能够显著抑制LX-2 细胞中Smad3、Smad4 及CollagenI mRNA 相对表达量。

图5 啤酒甾醇和腺苷对TGF-β1 诱导LX-2 细胞中相关基因转录水平的影响
2.5 蛋白免疫印迹
LX-2 细胞中Smad3、Smad4 蛋白表达条带见图 6,阳性组、腺苷组和啤酒甾醇组肝纤维化模型LX-2 细胞中Smad3、Smad4 蛋白条带较模型组浅,说明阳性组、腺苷组和啤酒甾醇组能够抑制 LX-2 细胞中Smad3、Smad4 蛋白相对表达量。LX-2 细胞中Smad3、Smad4 蛋白表达量见图7,与对照组相比,模型组LX-2 细胞中Smad3、Smad4蛋白相对表达较对照组显著上调( ****P<0. 01)。与模型组相比,阳性组、腺苷组和啤酒甾醇组 LX-2 细胞中Smad3、Smad4 蛋白相对表达水平均降低,其中啤酒甾醇组中Smad3 和Smad4 蛋白相对表达量显著下降(###P < 0.01,##P <θ, .01)。与阳性组相比,啤酒甾醇组中Smad3 和Smad4 蛋白相对表达量抑制作用不及阳性组,说明啤酒甾醇对诱导的LX-2 细胞肝纤维化相关蛋白具有显著抑制作用,但抑制效果不如复方鳖甲软肝片。
图6 蛋白表达条带

图7 啤酒甾醇和腺苷对TGF-β1 诱导LX-2 细胞中相关蛋白的相对表达量的影响

注:与对照组相比(**P <θ. .01);与模型组相比(##P <θ. .01,#P <θ, .01)
3 讨论
冬虫夏草是我国高原地区特有的名贵中药材 。现代医学研究表明,冬虫夏草多糖类成分具有免疫调节、肿瘤治疗、延缓衰老等药效;核苷类成分种类众多,如尿苷、肌苷、鸟苷、腺苷等,在癌症和抗病毒治疗中具有显着作用;甾醇类成分主要是麦角甾醇,具有抗肿瘤和调节细胞凋亡等功效;甘露醇又称虫草酸,具有抑制病菌、补肺益肾等功效[24]。关于冬虫夏草活性成分药理研究的报道多见于冬虫夏草可减缓肾纤维化[25]和发挥干预慢性阻塞性肺疾病的作用  。
。
近年来,由于药物、酒精、遗传、自身免疫等多种因 损伤现象较为普遍[27]。肝纤维化是各种慢性肝病向肝硬化进展的必经阶段 因此,本研究对冬虫夏草子实体有效组分中7 个单体化合物进 -2 细胞模型中所有单体化合物毒活性均较低,其中中腺 出较强的抑制作用 (p< 0.05)。这可能与腺苷和啤酒甾醇通过抑制 TG 和增殖,抑制其细胞外基质组分的过度分泌和积聚,促进其降解,从而发挥体外抗纤维化作用有关
肝纤维化的发展过程中,肝星状细胞(HSCs)活化是关键事件,HSCs 的活化与多种细胞内信号通路密切相关[30]。其中 TGF-β1/Samd 是经典的纤维化通路之一[31]。此外,活化的 HSCs 中α-平滑肌肌动蛋白升高并分大量细胞外基质,如胶原蛋白,其中以 I 型胶原为主(Collagen I)[32]。本研究通过实时荧光定量和蛋白免疫印迹检测分析发现啤酒甾醇能够显著降低 TGF-β1 诱导的 LX-2 细胞中 Samd3、Smad4、Collagen I 的 mRNA 相对表达量和显著抑制Smad3、Smad4 蛋白相对表达量,这与张效威[33]等人研究结果一致,说明啤酒甾醇具有抑制肝纤维化的潜力。啤酒甾醇抗肝纤维化的机制可能与其通过调节 TGF-β/Smads 中关键蛋白 Samd3、Smad4 的表达,从而减少肝组织中 collagen I 的沉积有关[34]。但啤酒甾醇抑制 Samd3、Smad4、Collagen I 相对表达量效果不及阳性组,说明啤酒甾醇抑制肝纤维化的效果不及复方鳖甲软肝片,这可能与化合物本身内在活性因素有关。
4 结论
本研究结果表明,冬虫夏草子实体单体化合物啤酒甾醇具有较强的抗肝纤维化作用,但作用效果不及复方鳖甲软肝片。啤酒甾醇抗肝纤维化作用可能与其抑制TGF-β诱导的LX-2 细胞的异常活化和增殖,通过调节TGF-β/Smads 中关键基因的转录表达,抑制其细胞外基质组分Collagen I 的过度分泌和积聚,促进 Collagen I 的降解,从而发挥体外抗纤维化作用有关。通过对冬虫夏草有效成分单体化合物的研究,为冬虫夏草后续的药理研究及合理利用提供科学依据。
参考文献:
[1].国家药典委员会. 中华人民共和国药典 2020 年版(一部)[M]. 北京:中国医药科技出版社, 2015: 115.
[2].钟民宽, 宋霞, 李永鹏, 等. 冬虫夏草的研究进展[J]. 青海科技, 2024, 31(06): 93-107.
[3].徐红, 董婷霞, 赵奎君, 等. 中药冬虫夏草的鉴别研究[J]. 中国药学杂志, 2014, 49(04): 283-286.
[4].高学敏主编. 中药学[M]. 北京:中国中医药出版社. 2007 年.
[5].国家药典委员会编. 中华人民共和国药典 2015 年版(一部)[M]. 北京:中国医药科技出版社, 2015年
[6].黄兆胜. 中药学[M]. 北京: 人民卫生出版社, 2002: 441.
[7].William H. arcia Santos, artha . ayorquin Torres, imsi ampos olalpa, et l. ynthesisof benzannulated spiroketals derived from stigmasterol and sitosterol by Pd ‐ catalyzedspirocyclization. MR nd ‐ray haracterization. valuation f ytotoxicity nd nti‐InflammatoryActivity [J]. Journal of Heterocyclic Chemistry.Volume 61, Issue 12. 2024.
[8].鲁斌, 全伟, 陈勇杏, 等. 桦褶孔菌中麦角甾醇类化学成分及其抗氧化活性研究[J]. 西南林业大学学报(自然科学), 2023, 43(06): 173-178.
[9].邹滨. 粗毛纤孔菌提取物的免疫活性及相关机制研究[D]. 长春:吉林农业大学, 2024.
[10].呼永华. 蒲公英的抗癌机理研究[J]. 西部中医药, 2018, 31(01): 132-134.
[11].祁一珊, 韩九林, 王青虎, 等. 肝纤维化临床诊断与蒙医药治疗研究进展[J]. 中国药业, 2025,34(09): 128-132.
[12]. 俞佳雯, 周薏, 林天龙, 等. 乙肝肝纤维化中西医研究进展[J]. 陕西中医, 2025, 46(02):273-276+280.
[13]. in en, iaolian iu, ejun ang, t l. anoparticle: athogenesis, nnovative iagnosis,and herapy f iver ibrosis[J]. hemistrySelect. olume 0, ssue . 025. P 202500446-e202500446
[14].Liangtao hao, aolan ang, hangjun heng. harmacotherapy f iver ibrosis nd epatitis:Recent Advances[J]. Pharmaceuticals. Volume 17 , Issue 12 . 2024. PP 1724-1724
[15].刘先治, 吴斌. Hepatology. 肝细胞来源 MASP1 活化肝星状细胞并促进肝纤维化[J]. 临床肝胆病杂志, 2024, 40(07): 1333.
[16].Wang , an , hang , t l.The lobal urden f iver isease: he ajor mpact f hina[J].Hepatology, 2015, 60: 2099-2108.
[17].Sinclair , Poltavskiy , Dodge , et l.Frailty is ndependently ssociated with ncreasedhospitalisation days in patients on the liver transplant waitlist[J]. World J Gastroenterol, 2017,23: 899-905.
[18].马雄, 邱德凯, 徐军, 等. 冬虫夏草多糖脂质体抗肝纤维化的实验研究[J]. 中国中医基础医学杂志,1999, (09): 29-31.
[19].任萍, 鞠萍. 对肝脏有保护作用单味中药[J]. 中国现代药物应用, 2011, 5(17): 76-77.
[20].李萍. 中医药抗肝纤维化研究进展[J]. 湖北中医杂志, 2001, (03): 52-54.
[21].任建平, 胡锡元. 中药免疫调节在抗肝纤维化中的作用[J]. 中医药研究, 2001, (06): 56-57.
[22].杨建华, 居博伟, 向雪滢, 等. 新疆假龙胆调控 TGF-β1/Smad 通路抑制肝星状细胞活化的作用机制[J]. 中华中医药杂志, 2022, 37(12): 7392-7396.
[23].崔兵兵, 李季, 刘可春, 等. 冬虫夏草多糖抑制肝纤维化作用机制的研究进展[J]. 中国实验方剂学杂志, 2019, 25(15): 228-234.
[24].付晓琳, 肖建, 牛乐军. 冬虫夏草通过调控 MAPK 通路减轻 CCl4 诱导的大鼠肝脏炎症和纤维化[J].中国药师, 2021, 24(09): 1657-1664.[
25].范卫锋, 邹园生, 李文佳, 等. 基于网络药理学和分子对接技术探讨冬虫夏草治疗肾纤维化的潜在作用机制[J]. 菌物学报, 2021, 40(11): 2995-3011.
[26].刘盈盈, 高雅琪, 豆改杰, 等. 基于网络药理学及分子对接技术探究冬虫夏草干预慢性阻塞性肺疾病作用机制[J]. 现代药物与临床, 2024, 39(06): 1398-1408.
[27]. 周洁清, 付蕾, 王萌, 等. 基于“阳化气,阴成形”及“虚”“瘀”理论论治气虚血瘀型肝纤维化[J/OL]. 辽 宁 中 医 药 大 学 学 报 , 1-9[2025-05-22]. http://kns.cnki.net/kcms/detail/21.1543.R.20250521.1805.002.html.
[28].廖玉, 王宁, 曹正民, 等. 中药调控 TGF-β1/Smad 信号通路防治肝纤维化的研究进展[J].中医药学报, 2025, 53(02): 102-107.
[29].邵益丹, 史婷婷, 赵艳梅, 等. 姜黄素及其衍生物对TGF-β 诱导的LX-2 细胞纤维化的抑制作用研究[J]. 中国现代应用药学, 2024, 41(13): 1750-1757.
[30].陈清枚, 陈维浩, 包宇杰, 等. CA17-1 通过调控 TGF-β1/Smad 信号通路改善肝纤维化[J/OL]. 中国现代应用药学, 1-12[2025-09-09]. https://doi.org/10.13748/j.cnki. issn1007-7693.20250389.
[31].张紫薇. 芥子酸通过 TGF-β1/Smad 信号通路抑制 TGF-β1 诱导的 LX2 细胞纤维化[D]. 延吉:延边大学, 2022.
[32].Xiong Y Li X un et al. bnormal ollagen deposition ediated by cartilage oligomericmatrix rotein n he athogenesis f ral ubmucous ibrosis[J]. nternational ournal f ral cience,2025, 17(03): 422-433.
[33].张效威, 刘宜杭, 张润东, 等. 中医药治疗酒精性肝病的组方用药规律及作用机制研究[J]. 中药新药与临床药理, 2024, 35(08): 1246-1254.
[34].宋海容, 邱建利, 李灿灿, 等. 丹参酮ⅡA 对胆道闭锁肝纤维化大鼠SMAD4 SMAD7 及I 型胶原蛋白的影响[J]. 安徽医学, 2024, 45(05): 537-541.
基金项目:互助县北山林场2024 年中央财政林业草原改革发展资金祁连山南坡天然林林下经营与碳汇能力提升技术集成推广项目(1008-0031201)
第一作者:赵天悦(1989-),女,汉族,青海民和人,在读硕士研究生,主要研究方向动植物分子进化与适应*通讯作者:谢惠春,男,博士,博士生导师,主要研究方向为动植物分子进化与适应






 京公网安备 11011302003690号
京公网安备 11011302003690号


