
- 收藏
- 加入书签
红连清肺颗粒对新型冠状病毒肺炎感染的抑制作用研究
摘要:目的:探究红连清肺颗粒对新型冠状病毒肺炎感染的抑制作用。方法:采用MTT法检测红连清肺颗粒的半数毒性浓度;采用细胞病变法检测病毒对MDCK细胞的半数感染量;通过治疗指数评价红连清肺颗粒对冠状病毒的抑制作用;采用死亡保护率与生命延长率考察红连清肺颗粒对冠状病毒感染小鼠的保护作用;采用血凝滴度与HE染色法研究红连清肺颗粒对冠状病毒感染小鼠的体内抑制作用;通过细胞因子和抗氧化指标的变化探究红连清肺颗粒抗病毒的作用机制。结果:药物对MDCK细胞的半数毒性浓度为1458μg/mL;冠状病毒的半数感染量为10-4.12;红连清肺颗粒的治疗指数为7.5,红连清肺颗粒和瑞德西韦均可抑制冠状病毒吸附后的复制增殖作用;红连清肺颗粒各剂量组和瑞德西韦组均可延长小鼠平均存活时间;红连清肺颗粒可显著降低TNF-α、IL-6、IFN-γ的含量,显著升高IL-10的含量;红连清肺颗粒可显著升高SOD的活力、降低MDA的活力。结论:红连清肺颗粒对新型冠状病毒OC43有较好的抑制作用,其作用机制可能与降低炎症细胞因子的表达,减轻冠状病毒造成的过氧化应激损伤有关。
关键词:红连清肺颗粒;冠状病毒;抑制作用
冠状病毒(coronaviruses,CoVs)为有包膜的单股正链RNA病毒,病毒粒子呈球形,基因组全长27~33kb,是目前已知基因组最大的RNA病毒。根据血清及遗传特性可进一步将冠状病毒分为α、β、γ、δ四个属,α和β属主要感染人类及哺乳动物[1,2]。目前发现能够感染人的冠状病毒共有7种,HCoV-229E和NL6属于α冠状病毒,而严重急性呼吸窘迫综合征、中东呼吸综合征冠状病毒(MERS-CoV)、新型冠状病毒(SARS-CoV-2)、HCoV-HKU1和HCoV-OC43属于β冠状病毒。目前国际上批准可紧急用于治疗SARS-CoV-2感染药物仅有奈玛特韦片/利托那韦片[3],急需储备更多抗病毒药物。
红连清肺颗粒由西藏藏医药大学博士生导师索朗其美教授根据《四部医典》古籍中的九味藿香雪莲汤变化而来,后经过国医大师金世元、王智森教授和陆付耳教授根据新型冠状病毒感染的临床病例情况,变化为现有的临床方剂。该方剂在临床上能够抑制病毒的复制、阻止病毒引起细胞病变、调节机体免疫功能、改善肺循环和镇痛抗炎等综合功效,且病毒很难对其产生抗药性。因此,本研究通过对红连清肺颗粒的体内、体外抑制作用试验,确定其对新型冠状病毒OC43(HCoV-OC43)的抑制作用,并初步探讨其可能的作用机制,为红连清肺颗粒抗新型冠状病毒的临床应用提供试验依据。
1、材料与试剂
1.1 药物与试剂
红连清肺颗粒:石家庄藏诺药业股份有限公司;对照药物瑞德西韦:购于美国Target Mol公司;噻唑蓝(MTT)和二甲基亚砜(DMSO)购自sigma公司;DEME培养基、膜蛋白酶和胎牛血清购自美国Hyclone公司;水合氯醛、甲醛、乙醇、二甲苯、伊红、苏木素、盐酸,均购于北京化学试剂公司;酶联免疫试剂盒购自ebiosience公司;超氧化物歧化酶检测试剂盒、丙二醛检测试剂盒,购于南京建成生物工程研究所。
1.2 动物
SPF 雌性BALB/c小鼠,6~8周龄,体重(20±2)g,购于湖北省实验动物研究中心,动物许可证号:CXK E2020-0018。饲养于湿度为50~70%的屏障环境。
1.3 仪器
小型冷冻台式离心机,美国Thermo Fisher Scientific公司;酶标仪,美国Bio-Rad公司,CO2细胞培养箱,美国Thermo Fisher Scientific公司;生物安全柜,美国Thermo Fisher Scientific公司;倒置显微镜,日本Nikon公司;电子分析天平,德国sartorius公司;微孔混匀仪,德国Eppendorf公司;去离子水纯水仪,德国Millipore公司;超低温冰箱,中科美菱低温科技有限责任公司;生物组织包埋机,浙江省金华市科迪仅器设备有限公司;轮转石蜡切片机,德国徕卡公司;摊片机,江省金华市科迪仪器设备有限公司;烤片机,天津爱华医疗器械有限公司。
2、方法
2.1、样品制备
2.1.1、红连清肺溶液制备
精密称取红连清肺颗粒,溶于100 mL热水中,涡旋使其充分溶解,冷却过滤,即得1mg/mL的母液,4℃保存备用。
2.1.1、瑞德西韦溶液
精密称取瑞德西韦,溶于80 mL热水中,涡旋使其充分溶解,即得1250 μg/mL 的母液,4℃保存备用。
2.2、红连清肺颗粒抑制 HCoV-OC43感染的体外研究
2.2.1、红连清肺颗粒与瑞德西韦对MDCK细胞存活率的影响
取对数生长期MDCK细胞,进行细胞计数,调整细胞密度为2×104个/mL,每孔200 μL接种于96孔板中,在5%CO2培养箱中培养24h。实验分为正常组(细胞+培养基)、瑞德西韦组(浓度分别为312.5、156.25、78.125、39.062 μg/mL)、红连清肺颗粒组(浓度分别为10000、5000、2500、1250、625、312.5、156.25、78.125、39.062 μg/mL),每组4个复孔,培养72 h后,在避光条件下,每孔加5 mg·mL-1 MTT溶液20 μL,混匀后置于CO2培养箱中继续孵育4 h,弃去各孔中上清液,加入150 μL DMSO,振荡混匀15 min,待其各孔中的紫色结晶完全溶解,570 nm处测OD值,用统计软件SPSS24.0对数据进行Probit回归分析,计算药物的半数毒性浓度(TC50)。
2.2.2、病毒对MDCK细胞的影响
取对数生长期MDCK细胞,进行细胞计数,调整细胞密度为2×104个/mL,每孔200 μL接种于96孔板中,在5%CO2培养箱中培养24h。实验分为正常组(细胞+培养基)、病毒组(101~1010),每组8个复孔,在5%CO2培养箱中培养。观察细胞病变,当细胞病变出现80~90%时,采用Reed-Muench法计算冠状病毒的半数感染量(TCID50)。
2.2.3、红连清肺颗粒对HCoV-OC43的抑制作用
取对数生长期MDCK细胞,进行细胞计数,调整细胞密度为2×104个/mL,每孔200 μL接种于96孔板中,在5%CO2培养箱中培养24h,加入100 μL(100TCID₅)冠状病毒,吸附1h后弃去上清液,随后再分别加入1250、625、312.5、156.25、78.125、39.062 μg/mL红连清肺颗粒,每孔100 μL,每组4个复孔。同时设病毒组 (细胞+病毒+培养液)、正常组(细胞+培养液)、红连清肺颗粒组、瑞德西韦组(浓度梯度为312.5、156.25、78.125、39.062 μg/mL),每组4个复孔。逐日观察细胞形态变化,当病毒对照孔细胞出现病变时,记录细胞病变结果,当病毒对照孔CPE在80%~90%时结束试验,MTT染色法测定细胞活性。试验分别重复3次。采用统计软件SPSS24.0对数据进行Probit回归分析,分别计算药物的半数有效浓度(EC50)。采用治疗指数(TI)作为评价指标,用于评价红连清肺颗粒对冠状病毒吸附后的复制增殖作,TI=TC50/EC50。病毒抑制率计算方法:
2.3、红连清肺颗粒抑制HCoV-OC43感染的体内研究
2.3.1、红连清肺颗粒对HCoV-OC43 感染 BALB/C 小鼠死亡的保护作用
雌性BALB/C小鼠适应性饲养5d后,随机分为6组,即空白组、病毒组、瑞德西韦组(100 mg/kg)、红连清肺颗粒低剂量组(1.5 g/kg)、红连清肺颗粒中剂量组(0.75 g/kg)、红连清肺颗粒高剂量组(0.375 g/kg)。红连清肺颗粒连续灌胃2d后,空白组滴鼻PBS溶液50μL/只,其他各组冠状病毒攻毒实验浓度10LD50(LD50为10-3.375)/50 μL,4h后给药,连续给药5天,空白组和模型组给予等体积的生理盐水;从感染当日开始连续观察14d,主要观察BALB/c小鼠的发病症状,记录死亡时间和死亡数,计算死亡率、死亡保护率和平均存活时间。
2.3.2、红连清肺颗粒对HGoV-OC43感染BALB/C小鼠所致肺炎的影响
2.3.2.1、分组及给药
分组给药同“2.3.1”。
2.3.2.2、红连清肺颗粒对HGoV-OC43感染BALB/C小鼠肺指数和肺指数抑制率
病毒感染5d后,禁食不禁水过夜12h后,收集肺组织,计算肺指数和肺指数抑制率。
2.3.2.3、红连清肺颗粒对HGoV-OC43感染BALB/C小鼠肺组织中血凝滴度的影响
各组随机取6个肺脏置匀浆器中加冷生理盐水[肺重(g)/生理盐水(mL)=1/9], 在冰浴中研磨制成匀浆,4℃离心后取上清,进行微量血凝试验。
2.3.2.4、红连清肺颗粒对HGoV-OC43感染BALB/C小鼠肺组织病理的影响
肺组织采用4%组织固定液固定48h;自来水冲洗固定液后梯度酒精脱水(75%,85%,95%Ⅰ,95%Ⅱ,100%I,100%II),然后进行组织透明(二甲苯I,二甲苯Ⅱ),浸蜡(蜡I,蜡II)后包埋;将包埋修整好的蜡块切片(片厚3 μm),60℃烤片后染色;HE染色(二甲苯Ⅰ,二甲苯Ⅱ脱蜡,过100%Ⅰ,100%Ⅱ,95%,85%,75%的梯度酒精,流水冲洗,苏木素染,流水冲洗,1%盐酸酒精分化,流水冲洗返蓝,伊红染液染色);将切片依次放入75%,85%,95%I,95%II,100%Ⅰ,100%Ⅱ梯度酒精,二甲苯Ⅰ,二甲苯Ⅱ中脱水透明,晾干,中性树胶封片;显微镜镜检,图像采集分析。
2.3.2.5、红连清肺颗粒对HGoV-OC43感染BALB/C小鼠肺组织中细胞因子水平的影响
各组随机取6个肺脏置匀浆器中加冷生理盐水[肺重(g)/生理盐水(mL)=1/9], 在冰浴中研磨制成匀浆,4℃离心后取上清,检测IL-6、IL-10、TNF-α与IFN-γ。
2.3.2.6、红连清肺颗粒对HGoV-OC43感染BALB/C小鼠血清中SOD和MDA的影响
感染5d后,禁食不禁水过夜12h后,收集血液,3000 rpm,离心10 min,分离血清,检测超氧化物歧化酶(SOD)活力和丙二酸(MDA)的含量。
2.4、统计方法
采用 SPSS 24.0对实验数据进行统计学分析,数据统计结果以均数±标准差(X̅±s)表示,组间数据采用单因素方差分析,当P<0.05为差异有统计学意义。
3、结果
3.1、冠状病毒HcoV-OC43对MDCK细胞的半数感染量(TCID50)
冠状病毒HCoV-OC43感染细胞后观察到病变:细胞变圆,出现空泡,细胞折光性增强,细胞之间拉网、皱缩、呈星状聚集成团、脱落,核固缩,碎裂,最后整个细胞破成碎片,而对照组中的MDCK细胞状如梭形或多边形的上皮细胞形态,生长良好,排列紧密,且培养液透明清亮,见图1。冠状病毒HCoV-OC43的TCID50为10-4.12/100μL。
3.2、药物对MDCK细胞存活率的影响
研究发现,红连清肺颗粒的浓度≥2500 μg/mL,细胞增殖缓慢,折光性发生改变,肿胀变圆,部分细胞贴壁能力下降,破碎,脱落,胞浆内颗粒增多,其细胞存活率低,红连清肺颗粒的浓度≤1250μg/mL,72h后和正常组细胞生长差异不大,存活率>75%。瑞德西韦药物浓度为312.5 μg/mL时,细胞存活率≥80%,其最大无毒浓度大于312.5μg/mL。采用SPSS24.0对数据进行Probit回归分析,药物对MDCK细胞的半数毒性浓度TC50为1458μg/mL。红连清肺颗粒对细胞毒性作用影响见表1。
3.3、红连清肺颗粒对HCoV-OC43的抑制作用
在药物的安全范围内,随着药物浓度的增加,药物抗冠状病毒的抑制率而增强,呈一定的量效关系,红连清肺颗粒和瑞德西韦均有明显抑制冠状病毒吸附后的复制增殖作用。
在未加药物的病毒感染细胞出现明显的CPE时,各浓度药物孔细胞存活数量与生长状态不同,但细胞均明显多于病毒组,红连清肺颗粒浓度高于312.5μg/mL和瑞德西韦高于78.12ug/mL时,视野内有50%以上细胞成活。红连清肺颗粒的半数有效浓度为212.2±19.2 μg/mL,其治疗指数(TI)为7.5,瑞德西韦的半数有效浓度为69.8±8.3 μg/mL,其治疗指数(TI)为>4.5。结果见表2。
3.4、红连清肺颗粒对HCoV-OC43感染BALB/c小鼠死亡的保护作用
在14d观察期内,空白组小鼠没有出现死亡,死亡率为0,病毒组小鼠的死亡率为86.6%,瑞德西韦组小鼠的死亡率为26.6%,具有明显的死亡保护作用(P<0.01),红连清肺颗粒中剂量组小鼠死亡率为40%(P<0.01)。其他几组与病毒对照组相比,无统计学意义(P>0.05)。
病毒组小鼠存活时间为9.0d,与空白组相比,小鼠平均存活时间极显著降低(P<0.01)。与病毒组相比,红连清肺颗粒各剂量组和瑞德西韦组小鼠平均存活时间明显延长,瑞德西韦组小鼠平均存活时间为12.5d,红连清肺颗粒中剂量组小鼠平均存活时间为12.0d,两组与病毒组相比小鼠平均存活时间极显著延长(P<0.01)。其他几组与病毒组相比,无统计学意义(P>0.05)。结果见表3。
3.5、红连清肺颗粒对HCoV-OC43感染小鼠所致肺炎的影晌
3.5.1、红连清肺颗粒对HCoV-OC43感染小鼠肺脏指数的影响
红连清肺颗粒对于HCoV-OC43感染小鼠5d后肺指数的变化结果显示:与空白组相比,病毒组肺指数极显著升高(P<0.01)。与病毒组相比,瑞德西韦组和红连清肺颗粒中剂量组肺指数极显著降低(P<0.01),红连清肺颗粒低剂量组和红连清肺颗粒高剂量组肺指数显著降低(P<0.05)。结果见由表4。
3.5.2、红连清肺颗粒对HCoV-OC43感染小鼠肺组织中血凝滴度的影响
利用红血球凝集试验(HA)测定HCoV-OC43感染小鼠后在肺组织中的血凝效价,反映冠状病毒的复制情况。连续灌胃不同剂量的药物5d后,与病毒组相比,药物组小鼠肺组织血凝滴度均极显著降低(P<0.01),表明各组药物均有不同程度的抑制冠状病毒的效果,瑞德西韦组血凝滴度最低,抑制冠状病毒效果最好。红连清肺颗粒各药物组血凝滴度中剂量组低于高剂量组和低剂量组,说明三个剂量组中,红连清肺颗粒中剂量组抗冠状病毒组效果更好。结果见图2。
3.5.3、红连清肺颗粒对HCoV-OC43感染BALB/c小鼠的肺组织病理的影响
红连清肺颗粒对于HCoV-OC43感染小鼠5d后病理形态学结果显示:HE染色观察正常组小鼠肺组织结构,终末细支气管部分向周边伸展,构成呼吸细支气管,再分支成肺泡管(腺泡)和肺泡,各级支气管结构清楚,肺泡组织内基本没有浸润的炎性细胞渗出。肺泡壁毛细血管充斥着红细胞。各级支气管周围间质有肺动脉、肺静脉、淋巴组织和疏松结缔组织(见图3a)。
病毒组大部分肺组织肺泡结构破坏,部分肺组织实变区融合,肺泡隔增厚,肺泡腔和间质内炎细胞浸润,病变较重,毛细血管充血(见图3b箭头B)肺泡破坏,炎性细胞浸润(见图3b箭头A)。瑞德西韦组连续7d灌胃,可明显改善肺部炎性病变程度,炎性细胞浸润明显减少或消退,接近正常肺组织结构(见图7c箭头)。
红连清肺颗粒不同剂量组连续灌胃7d后,不同程度的改善了肺组织的病变,由切片照片可看出中剂量组约1/2肺组织炎性细胞明显减少,未见充血出血(见图4d箭头)。低剂量治疗后效果约1/3肺组织炎性细胞明显减少,其余的肺组织炎细胞减少(见图7f箭头)。高剂量组约1/3肺组织炎性细胞明显减少,抑制作用不如中剂量组明显(见图7e箭头)。
3.5.4、红连清肺颗粒对HCoV-OC43感染BALB/c小鼠的肺组织中细胞因子水平的影响
冠状病毒感染小鼠5d后,与空白组相比,病毒组TNF-α和IL-6极显著升高(P<0.01);与病毒组相比,红连清肺颗粒中剂量组和低剂量组TNF-α极显著降低(P<0.01),红连清肺颗粒中剂量组IL-6显著降低(P<0.05),其他组均有不同程度的降低,但无统计学意义(P<0.05);红连清肺颗粒高、中、低剂量组两两比较TNF-α和IL-6无统计学意义(P<0.05)。病毒组与空白组相比,IL-10极显著降低(P<0.01);与病毒组相比,灌胃给药后,红连清肺颗粒中剂量组IL-10显著升高(P<0.05),其他组均有不同程度的升高,但是没有统计学意义(P<0.05);红连清肺颗粒高、中、低剂量组两两比较IL-10无统计学意义(P<0.05)。与空白组相比,病毒组IFN-γ极显著降低(P<0.01);与病毒组相比,红连清肺颗粒中、低剂量组IFN-γ极显著升高(P<0.01),红连清肺颗粒高剂量组IFN-γ显著升高(P<0.05);红连清肺颗粒高、中、低剂量组两两比较IFN-γ无统计学意义(P<0.05)。结果见图4。
3.5.5、红连清肺颗粒对HCoV-OC43感染BALB/c小鼠血清中SOD和MDA的影响
与空白组相比,病毒组SOD活力极显著降低(P<0.01);与病毒组相比, 红连清肺颗粒中剂量和低剂量组SOD活力极显著升高(P<0.01),红连清肺颗粒高剂量组SOD活力显著升高(P<0.05);红连清肺颗粒高、中、低剂量组之间两两比较,红连清肺颗粒中剂量组和红连清肺颗粒低剂量组SOD活力极显著高于红连清肺颗粒高剂量组(P<0.01)。与空白组相比,病毒组MDA含量极显著升高(P<0.01);与病毒组相比,红连清肺颗粒高、中、低剂量组物组MDA极显著降低(P<0.01);红连清肺颗粒高、中、低剂量组之间两两比较MAD含量没有统计学意义(P<0.05)。比较结果见表5。
4、讨论
冠状病毒入侵机体后,病毒在宿主细胞内复制然后入血,形成病毒血症。在病毒作用于机体后,机体免疫细胞产生了免疫应答,进而产生大量生物学活性的小分子蛋白质一细胞因子。研究发现新冠肺炎死亡患者脓毒症的发生率远高于轻症患者,促炎细胞因子(IL-1β、IL-6、IFN-γ、TNF-α),趋化因子(CCL-2、CCL-3、CCL10)等的大量释放导致失控性全身炎症反应综合征。研究表明,重型新冠肺炎患者血清中IL-1β、IL-6、IL-8、IL-10和TNF-α水平明显增加,并与患者病程发展密切相关[4]。其中诱发病毒性肺炎患者的关键炎症因子主要包括TNF-α和IL-6[5]。此外,IL-6指标变化可引做COVID-19重型、危重型的评估[6]。CD4+T细胞与CD8+T细胞在HAdV清除过程中发挥着重要作用。CD4+T细胞可以分泌IFN-γ、TNF-α、IL-17A等细胞因子参与抗病毒免疫[7]。有研究表明,塞内卡病毒SVV可通过PERK、ATF6及AKT-AMPK-mTOR途径诱导细胞自噬,引起IL-6、TNF-α和IFN-γ等炎症因子分泌水平升高[8]。宿主细胞可通过自噬降解病毒成分、病毒颗粒等,还可触发机体的免疫反应,诱导IFN-β、IL-8等炎症细胞因子释放,从而发挥抗病毒作用[9]。冠状病毒作用靶器官肺脏,引起免疫细胞相互作用,伴随自由基的明显增加,导致正常的组织细胞受损。因此氧自由基与抗氧化剂间保持动态平衡对于维持组织细胞的正常结构及功能是极其重要的。SOD有抗炎、抗病毒及抗氧化等多种功能,是机体内常见的抗氧化酶,主要清除超氧阴离子[10]。GSH-Px可消除机体内过多的过氧化物,使体内自由基保持在低水平,维持生物膜的功能。脂质过氧化时产生的MDA会导致机体生物膜的结构异变与功能紊乱,MDA含量一定程度上可反映机体受自由基损害的程度。机体内的SOD与GSH-Px形成具有抗氧化能力的保护系统,可抵御氧化物的干扰和损伤[11,12]。
综上所述,体内、体外试验表明红连清肺颗粒对新型冠状病毒感染有显著的抑制作用。红连清肺颗粒可增加病毒感染后小鼠的存活率、调节细胞因子分泌,减轻冠状病毒造成的过氧化应激损伤等方面具有一定抗病毒的功能。今后可从整体化学物质组出发,系统筛选其抗病毒的活性组分或成分,结合代谢组学、蛋白质组学及转录组学等系统生物学手段探究其作用机制,为红连清肺颗粒的临床应用提供实验依据。
参考文献
[1] WANG D, HU B, HU C, et al. Clinical Characteristics of 138 Hospitalized Patients With 2019 Novel Coronavirus–Infected Pneumonia in Wuhan, China[J]. Jama, 2020, 323(11).
[2] CAROD ARTAL F J. Complicaciones neurológicas por coronavirus y COVID-19[J]. Revista de Neurología, 2020, 70(09).
[3] WANG J, LI H. Editorial of Special Column on Antiviral Drug Discovery and Pharmacology[J]. Acta Pharmaceutica Sinica B, 2022, 12(4): 1540-1541.
[4] 祝晟. 从过度炎症反应认识重症新冠肺炎[J]. 实用休克杂志(中英文), 2020, 4(06): 331-333.
[5] DARIF D, HAMMI I, KIHEL A, et al. The pro-inflammatory cytokines in COVID-19 pathogenesis: What goes wrong?[J]. Microbial Pathogenesis, 2021, 153.
[6] HUANG Y-F, BAI C, HE F, et al. Review on the potential action mechanisms of Chinese medicines in treating Coronavirus Disease 2019 (COVID-19)[J]. Pharmacological Research, 2020, 158.
[7] HUTNICK N A, CARNATHAN D, DEMERS K, et al. Adenovirus-specific human T cells are pervasive, polyfunctional, and cross-reactive[J]. Vaccine, 2010, 28(8): 1932-1941.
[8] 李媛媛, 马旭升, 等. A型塞内卡病毒激活炎症因子表达及诱导细胞焦亡[J]. 中国兽医科学, 2022, 52(05): 586-594.
[9] HOU P, YANG K, JIA P, et al. A novel selective autophagy receptor, CCDC50, delivers K63 polyubiquitination-activated RIG-I/MDA5 for degradation during viral infection[J]. Cell Res, 2021, 31(1): 62-79.
[10] 吴远彩, 李日美, 申光荣, 等. 小肽对凡纳滨对虾生长、抗氧化能力、非特异性免疫及肠道菌群结构的影响[J]. 广东海洋大学学报, 2021, 41(05): 1-9.
[11] 史宝, 柳学周, 刘永山, 等. 盐度渐变对黄条鰤消化酶和超氧化物歧化酶活力及甲状腺激素的影响[J]. 中国海洋大学学报(自然科学版), 2020, 50(01): 48-56.
[12] SUI Y, HUANG X, KONG H, et al. Physiological responses to salinity increase in blood parrotfish (Cichlasoma synspilum ♀ × Cichlasoma citrinellum ♂)[J]. SpringerPlus, 2016, 5(1).
注:“河北省省级科技计划资助”(英文标注:“S&T Program of Hebei”);项目编号:20272501D






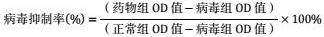





 京公网安备 11011302003690号
京公网安备 11011302003690号


