
- 收藏
- 加入书签
基于透明质酸构建的超分子系统应用研究进展
摘要:超分子化学是制备生物材料的一项重要技术。超分子具有一些独特的优势,能融入可降解大分子骨架,对各种生物刺激的智能响应,以及易于整合多种生物功能, 在生物医学显示出巨大的应用潜力。透明质酸(hyaluronic acid, HA)在人体中参与重要的生理过程,也能共价偶联大量客体分子,为主体和客体分子自组装形成超分子提供支架或载体。本文概述了基于HA构建的超分子系统在药物传递、生物成像和组织工程的应用。
关键词:透明质酸;超分子;药物递送;生物成像;组织工程
透明质酸(Hyaluronan, HA)是一种线性阴离子聚合物,由D -葡萄糖醛酸和N -乙酰D -葡萄糖胺通过交替的β – 1,3和β – 1,4糖苷键连接。它是细胞外基质(extracelluar matrix, ECM)、玻璃体和脊椎动物滑膜液的主要成分,现在越来越多地通过微生物发酵产生。HA与水分子紧密结合,形成大量水合凝胶,调节生物液体粘弹性。在透明质酸粘素家族中,CD44和透明质酸介导的运动受体(receptor for hyaluronic acid-mediated motility,RHAMM)跟HA生物活性密切相关,它们参与多种细胞过程,如粘附、活化、迁移和增殖,还介导HA的生物降解。HA与CD44和RHAMM的相互作用可诱导酪氨酸激酶、蛋白激酶C、PI3K、丝裂原活化蛋白激酶 (mitogen-activated protein kinase , MAPK)、NF-kB和RAS的激活。此外,HA与CD44的结合涉及细胞凋亡和细胞增殖。CD44与两个酪氨酸激酶紧密结合,即p185-HER2和c-Src激酶,因此HA具有刺激CD44相关的p185-HER2酪氨酸激酶活性的能力,从而导致肿瘤细胞的生长增加。HA的信号传导及生物功能跟它的分子量密切相关。HA是目前临床眼科手术常用的粘弹剂,也能促进伤口愈合和组织的再生。它易于化学修饰,能跟环糊精(cyclodextrin, CD)和葫芦脲(Cucurbituril, CB)等常见的大环主体分子偶联,充当主体分子的支架或载体;金刚烷等客体分子能选择性地识别客体分子,并通过非共价键自组装,从而形成基于HA骨架的聚合物型超分子系统,具有药物传输、组织工程和生物成像等用途。
1药物输送
HA和CD 等许多构建超分子系统的模块或片段是无毒性,且非共价相互作用代替了自由基或偶联试剂介导的化学反应,大大提高了给药系统的安全性。此外,含HA的超分子系统的形成或组装能在生理环境中进行,呈现良好的水溶性,使它们适于体内应用。而且,通过调整超分子模块的密度、官能团和响应因素可以实现对药物的控释。
1.1基于分子识别的给药系统
设计超分子药物传递载体的一个考虑因素是生理环境中潜在的蛋白质或离子等竞争性结合。竞争相互作用可以影响超分子的力学性能或改变系统对负载药物的释放特性。在设计药物载体时利用分子识别可以减少这种机会。以HA等聚合物网络作为载体,客体分子通过点击反应等方法固定在聚合物主链或侧链上。β- CD具有亲水的外表面和亲脂的中心腔,是典型的药用辅料,能识别大位阻的疏水性金刚烷(adamantane, Ad),它们的相互作用可以用来交联功能化聚合物,组装成适合控释药物的超分子体系,并具有对药物的高负载能力;癌细胞表面过度表达HA的CD44受体,使得药物向癌细胞递送具有了靶向性。
1.2 刺激响应性给药系统
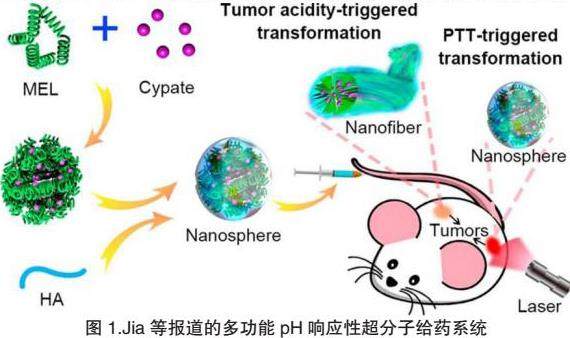
当主客体携带刺激响应因素时,超分子系统拥有了对外部刺激响应的特征。光是常用的刺激因素,依赖光敏试剂,不仅有助于自组装形成超分子,还有改善药物的安全性和有效性。Jia等开发了一种独特的超分子策略,将蜂毒肽(Melittin, MEL)转化为一种安全的、自追踪、肿瘤靶向的纳米药物。光敏剂二氢卟酚e6(chlorin, Ce6)能与蜂毒蛋白形成稳定的络合物,通过屏蔽蜂毒蛋白的正电荷,显著降低其溶血活性。表面的HA涂层使整个纳米复合物具有靶向肿瘤能力。该给药系统可快速招募到癌细胞表面并通过破坏细胞膜结构导致细胞死亡,而它对正常细胞的几乎无细胞毒性。在激光照射下,光敏剂通过产生氧自由基能进一步增强肿瘤球状体模型的消融[14]。他们还发展了pH响应的超分子给药系统(见图1),由MEL、荧光染料cypate和HA通过自组装形成。在pH 7.4环境中,该组装体为粒径约50 nm的带负电纳米球,有较长的血浆半衰期;当到达肿瘤区时,会在瘤内微酸性环境的触发下从纳米球原位转变为纳米纤维,这大大延长了药物在肿瘤组织内的富集时间。此外,大鼠肿瘤模型试验还证明了该纳米纤维的形成能够抑制癌细胞的迁移和侵袭,从而有效缓解了肿瘤向肺部的转移。在cypase介导的光热治疗过程中,近红外激光照射可将纳米纤维光降解为更小的纳米球(约25 nm),使负载的蜂毒肽能够穿透肿瘤,从而实现有效的治疗。
由于许多物理、化学和生物刺激能够引发分子的自组装,可以整合这些外部可观察的触发因素,开发化学或生物传感器,能建立经济和快速的诊断和治疗方案。
例如,炎症性肠病迫切须要创新的治疗方法,理想的口服结肠给药系统应该在改善肠道稳态的同时,最大限度地提高结肠部位特异性药物释放的效率。由于葫芦脲能跟多种客体分子形成稳定的复合物,在构筑光触发超分子给药系统有应用前景 。Cheng等将CB与色氨酸化的壳聚糖先复合,并在介孔二氧化硅纳米颗粒表面与偶氮苯官能化的HA自组装形成超分子。肠道中的微生物会产生的偶氮还原酶,能分解偶氮苯,导致超分子解体,使得药物释放,从而最大限度地减少它们在到达目标部位前的过早释放。该超分子药物传递系统包含色氨酸衍生物,通过激活微生物的色氨酸代谢,触发结肠芳基烃受体激活,促进上皮屏障完整性,调节炎症细胞因子的产生,从而改善肠道稳态,纠正了传统药物递送系统诱导的急性结肠炎的肠道失调。
2生物成像
分子影像学是诊断学中不可缺少的工具,具有重要的临床意义;另外,药代动力学、靶部位积累、药物释放和治疗效果可以使用无创成像技术进行定量监测。基于主体分子CD或CB跟HA组装的超分子有优越的成像能力。
荧光成像是目前生物学研究中重要的流行方法,它为细胞的结构组织、复杂的细胞事件和生物分子动态装配提供了新的视角和精确的细节。将荧光成像和超分子化学结合起来,是一种直接而有效的方法,可以区分、描述和记录细胞环境中超分子组装的行为。一般来说,合成的荧光团体积小,在整个可见光光谱中呈现出多种颜色,易于进行化学修饰,并具有光泽明亮、光稳定性和光开关性等优点。因此,它们极大地促进超分子生物功能材料的广泛应用。
聚集诱导发射(aggregation induced emission, AIE)在细胞成像中的应用是超分子化学的研究热点。AIE材料与常规荧光试剂相比,如高固体量子产率、耐光性、良好的生物相容性、无随机闪烁及强大的抗光漂白,共同促进AIE材料荧光成像技术的应用。在各种AIE材料中,具有聚集和荧光行为的四苯基乙烯(Tetraphenylethylene, TPE)易于合成和修饰,是一种用于亚细胞、细胞或组织水平的非侵入性和高亮度荧光成像的共轭小分子。HA常被用作聚集诱导支架、AIE的开启剂和靶向载体。具有AIE作用的超分子组装被构建为两个阶段,其中金刚烷修饰的TPE发出微弱的荧光,然后在添加β-环糊精修饰的透明质酸之后,形成的纳米颗粒增强了AIE荧光以用于靶向癌细胞成像。
Zhang等报道了还原响应荧光超分子系统,它由二硫键连接Ada化的萘酰亚胺和喜树碱(camptothecin,CAP)前药及β-CD修饰的HA构建,能够靶向细胞和在特定位点控制药物释放。该系统有极佳的CAP的水溶性、生物相容性和靶向性; HA受体介导的细胞吞噬导致系统选择性被癌细胞摄取,随后二硫键对氧化还原环境的快速响应,允许药物在癌细胞内释放;萘酰亚胺是一种有用的荧光响应元件,在内源性谷胱甘肽裂解二硫键后,其发射光可以从蓝色红移到绿色,被用作荧光响应报告器来监测药物释放。
3组织工程
组织工程是旨在创造用于移植的人造组织和器官。这一过程需要合适的支架为细胞播种、增殖和分化提供三维支持。为满足组织工程的需要,所设计的支架应具有以下关键特性:具有良好的生物相容性和生物降解性,可在体内应用;用于细胞迁移和增殖的高孔结构;与周围组织具有良好的机械强度和弹性;细胞与生物材料能相互作用。化学交联策略制备的水凝胶往往有很大毒性,而超分子水凝胶已被认为是组织工程的一种候选材料,具有自愈合和剪切稀化行为,且更具生物安全性。能无缝填充多个不规则关节炎软骨缺损。一旦注入,凝胶状态可以自我恢复,从而防止被封装细胞的泄漏和沉淀,可用于软骨缺损治疗。透明质酸是软骨ECM的主要成分,有较高的吸水能力,增加软骨中抗炎分子的表达,能偶联主体分子和客体分子,是二者相互作用的载体,并充当人间充质基质细胞(human mesenchymal stem cells, hMSC)的良好支架,在大鼠试验中能促进软骨再生。软骨再生工程可以结合基因治疗的策略,表达促软骨生成的蛋白活性因子。例如Rey-Rico等设计合成的超分子水凝胶不仅作为支架有良好的粘弹性,能承受高压灭菌条件而不变性;还可以持久地递送重组腺病毒载体,并在凝胶中的hMSCs实现转染,与裸载体相比凝胶具有更高的转基因表达水平。
考虑到骨软骨成分的复杂,张等开发了具有诱导干细胞分化和释放的仿生双相骨软骨支架(biomimetic biphasic osteochondral scaffold,BBOS)。BBOS中的软骨再生层包含超分子透明质酸水凝胶,可模拟软骨的组成,控制生肌素(人间充质干细胞分化为软骨细胞的诱导剂)的释放。此外,采用3D打印的羟基磷灰石的支架作为骨再生层,释放阿仑膦酸盐(成骨细胞的诱导剂)。与无药物的支架相比,BBOS中的MSCs可促进分化成软骨细胞和成骨细胞。大鼠体内试验表明,BBOS显著促进软骨或骨在各自层再生。
超分子化学能够调谐生物材料的性质,模拟ECM的动态和粘弹性特性。然而,超分子键的非共价性质使水凝胶本质上很弱,在应力作用下会发生变形。限制了它们在生物医学的应用。将超分子交联和共价交联相结合,可以开发出具有较高强度的水凝胶。与普通的HA水凝胶相比,复合水凝胶能促进细胞粘附和增殖,增强软骨相关基因表达和基质分泌。开发模拟ECM纳米纤维形貌的生物材料存在未满足的需求。HA用甲基丙烯酸酯改性后,再经过电纺丝和纤维光交联,以AD或β-CD引导超分子纤维状水凝胶组装,呈现良好的力学性质。封装在纤维水凝胶中的hMSC在注射后和培养7天后表现出令人满意的生存能力(> 85%)。
4结语
总之,HA是构建超分子的良好天然生物大分子,能服务于药物输送、组织工程和生物成像。然而,大部分超分子类型仅用于体外试验,实现临床应用还有很长的路要走,未来研究应该包括生物安全性评价及药代动力学。从小分子前体制备高分子材料的策略通常需要繁琐或低产量的工艺程序,提高这些合成的规模和效率是重要的考虑因素。目前的HA超分子系统的形成主要基于主体对客体的识别,存在稳定性差、结构简单和功能单一等缺点。在同一系统中结合多个非共价相互作用有助于提高其力学性质和稳定性。特别是不同的非共价相互作用的协同效应能使超分子在不同刺激下具有多种性质和智能响应,有更大的生物医学应用潜力。
参考文献:
[1]Passi A, Vigetti D. Hyaluronan as tunable drug delivery system [J]. Adv Drug Deliv Rev, 2019, 146: 83-96.
[2]Gupta RC, Lall R, Srivastava A, et al. Hyaluronic acid: molecular mechanisms and therapeutic trajectory [J]. Front Vet Sci, 2019, 6:192.
[3]Kovačević J, Prucková Z, Pospíšil T, et al. A new hyaluronan modified with beta-cyclodextrin on hydroxymethyl groups forms a dynamic supramolecular network[J]. Molecules, 2019, 24(21):3849.
[4]Elamin KM, Yamashita Y, Higashi T, et al. Supramolecular complex of methyl-beta-cyclodextrin with adamantane-grafted hyaluronic acid as a novel antitumor agent [J].Chem Pharm Bull (Tokyo), 2018, 66(3): 277-285.
[5]Singh P, Chen Y, Tyagi D, et al. beta-Cyclodextrin-grafted hyaluronic acid as a supramolecular polysaccharide carrier for cell-targeted drug delivery [J].Int J Pharm, 2021, 602: 120602.
[6]Yao YR, Jin YJ, Jia X, et al. Construction of hyaluronic acid-covered hierarchically porous MIL-nanoMOF for loading and controlled release of doxorubicin [J]. Chemistry, 2021, 27(9):2987-2992.






 京公网安备 11011302003690号
京公网安备 11011302003690号


