
- 收藏
- 加入书签
地市级医疗器械不良事件监测技术创新应用研究
摘要:目的 对医疗器械不良事件监测技术应用进行研究分析,总结取得的成效和存在的问题,为不断完善监测技术,提高医疗器械风险发现、评估、防控能力奠定基础。方法 通过整理2016-2020年期间河源市医疗器械不良事件报告,建立基础数据库进行统计分析,发现存在问题,创新监测技术,设计规范记录本和工作手册、举办监测技术应用专场推广、开展质量评估会等方法,推动全市各级使用单位积极上报医疗器械不良事件报告表,提高报告表质量。结果 对比采取监测技术应用前(2016年1月-2020年12月)与采取监测技术应用后(2023年1-12月)的数据,医护人员报告上报意识和医疗器械不良事件报告表的数量和质量明显提高、安全监测工作质量持续提升,有效保障公众用械安全。结论 不断完善监测措施、推广监测技术,提高医疗机构的发现风险、控制风险的意识,进一步推动监测发现医疗器械风险预警和提高处置能力,切实发挥安全监测作用,为人民群众用械安全筑牢坚实的屏障,保障公众生命安全和身体健康。
关键词: 医疗器械;不良事件监测;监测技术
[Abstract] Purpose: To study and analyze the application of adverse event monitoring technologies for medical devices, summarize the achievements and existing issues, and lay a foundation for continuously improving monitoring techniques to enhance the ability to detect, assess, and control risks associated with medical devices. Methods: By sorting adverse event reports of medical devices in Heyuan City from 2016 to 2020, a basic database was established for statistical analysis to identify existing problems. Innovative monitoring technologies were introduced, including the design of standardized record books and manuals, specialized promotional sessions on monitoring technology applications, and quality assessment meetings. These initiatives encouraged all levels of usage units in the city to actively report adverse event forms for medical devices, thereby improving the quality of these reports.Results: Comparing the data before (January 2016 to December 2020) and after (January to December 2023) the application of monitoring technologies, there was a significant improvement in the awareness of reporting among healthcare personnel, and in the quantity and quality of adverse event reports for medical devices. The quality of safety monitoring work continuously improved, effectively ensuring the safety of public medical device usage. Conclusion: Continuously improving monitoring measures and promoting monitoring technologies enhances the awareness of risk detection and control in medical institutions. This further improves the capability for early warning and handling of medical device risks, effectively playing a role in safety monitoring, thereby establishing a solid barrier for the safe use of medical devices and protecting public health and safety.
[Key words] Medical Devices; Adverse Event Monitoring; Monitoring Technology
医疗器械安全事关人民群众生命安全和身体健康,是严肃的政治问题、基本的民生问题、重大的经济问题、严谨的技术问题。而医疗器械不良事件监测是我国上市后医疗器械开展风险管理的重要手段,因此做好医疗器械不良事件的持续监测和再评价工作尤为重要[1]。2018年,国家市场监督管理总局、国家卫生健康委员会以第1号令的形式公布《医疗器械不良事件监测和再评价管理办法》[2],为更好的开展医疗器械不良事件监测工作提供了政策导向。本文通过从安全监测的视角,采取多形式监测技术应用措施,推动全市各级使用单位积极上报医疗器械不良事件报告表,保障报告数据的真实、完整、准确,推动医疗器械使用风险发现、评估、防控,为市场监管及政策制定提供强有力的支撑,具有显著社会和经济效益。
1.资料来源
通过随机抽取河源市2016年1月-2020年12月在国家医疗器械不良事件监测信息系统上报审核状态为“待审核、审核通过”的1022例医疗器械不良事件报告,采取回顾性研究和对比方法,根据国家药品监督管理局制定的《医疗器械分类目录》,对报告中所涉及的医疗器械进行分类,并对医疗器械不良事件报告来源、报告事件分布情况、事件伤害程度、报告缺失项目情况进行规范化,录入 Excel 表格从而形成河源市医疗器械不良事件报告基础数据库。通过数据统计得出1022例报告均来自使用单位,占比100%,报告表季度均衡度为0.51,事件伤害程度为严重伤害的报告157份,占比15.36%,报告表中联系地址、联系电话、规格/型号、产品批号/编号、有效期、事件原因分析描述等项目缺失较多。
2.医疗器械不良事件监测技术应用方法
2.1设计规范记录本
报告表内容偏多、不懂如何填写、需要耗费很长时间影响其他工作等问题是基层医护人员日常普遍的认识,为解决这些问题,通过以线上系统填报项目内容为基础,广泛征求临床医护人员、监测员等相关人员意见,对报告项目进行简化,保留上报系统所需的必填信息,包括医疗器械基本情况、不良事件情况和使用情况等,增加了初步处置情况和经手人签名,形成较为客观、科学的改良版《医疗器械不良事件报告表》,并印制成记录本,发放到全市163家医疗机构医护人员使用,方便医护人员发现不良事件时能及时登记,方便信息收集、资料归档、便于备查。
2.2设计工作手册
针对常见的医疗器械不良事件,临床科室通用医疗器械品种及对应的不良事件临床表现,归纳整理出科学、全面的《医疗器械不良事件监测与报告工作手册》,该手册内容有监测与报告的相关定义,明确报告原则、报告范围、严重伤害定义与判定和严重报告类型,科室常用的医疗器械类别及对应的不良事件主要表现,方便应用于医院各个科室对照手册上报不良事件,提高工作效率,具有重要的指导价值。
2.3举办监测技术应用专场推广
针对监测技术推广范围及人员选择,统一规划,分布实施。一是召开专项会议。根据上报数据情况及技术应用推广情况,适时召开监测工作推进会和技术应用推广会,进一步提高医疗机构对监测工作的重视度及对开展不良事件监测工作的支持力度,保障监测技术应用工作高质量完成。二是举办形式多样的培训。组建监测培训讲师团,拓充培训师资队伍,点面结合,提高培训效果。根据人群的不同,面向县镇级监管监测人员、医疗器械使用单位、涉械企业分别开展针对性的培训,如监测上报基础知识培训、全市能力提高班、县区专场培训、风险监测培训等,进一步提高各级监测人员法律法规的熟悉度、监测业务知识的理解度、上报不良事件的认知度;鼓励医疗机构积极开展院内培训,将医疗器械不良事件监测内容纳入院内培训计划,特别是针对急诊科、检验科、手术室、输液室等高频用械的科室人员,将监测意识渗透到临床一线[3]。三是采取行政干预。以目标为导向,适时到医疗机构开展工作指导,指导监测上报单位根据自身实际制订医疗器械不良事件监测工作制度,将责任落实到人,做到用制度规范工作,促进单位机制完善,消除医疗机构对不良事件上报的疑虑,提高医护人员上报积极性,保证监测队伍稳定,保障监测质量。
2.4举办质量评估会
报告数量的不断增长为监测工作提供了“量”的基础,但是报告的“质”是报告可利用性的决定因素,是安全性监测与评价工作的基础[4]。为了评估监测报告水平,提高报告表信息利用及预警能力,每季度针对性开展县区医疗器械不良事件报告表质量评估。邀请各医疗机构监测技术骨干对报告表的真实性、准确性、完整性、及时性进行质量评估,评估的报告表为我市在国家平台上报的报告按类型(一般报告表和严重报告表)随机抽样。为评估监测骨干发放详细的评价标准进行报告表评估,并汇总得分,进行分析反馈。通过质量评估,较为客观全面体现了我市医疗器械不良事件报告表质量现状,同时也加深了各骨干对上报要求和审核标准的理解,切实有效改善报告表填报项目不完整、不良事件发生的原因分析不够深入的问题,有力推动了报告表质量提高。
3.实施监测技术推广前后数据对比
3.1医疗器械不良事件上报数量及报告来源
统计2019-2023年国家系统上报审核状态为“待审核、审核通过”医疗器械不良事件报告表数,2019年873份,2020年952份,2021年1416份,2022年1465份,2023年1590份,报告表来源均为医疗机构使用单位。
3.2医疗器械不良事件报告质量
从国家不良事件监测信息系统获取河源市2023年1月-12月上报审核状态为“待审核、审核通过”的1590例医疗器械不良事件报告数据,对报告表上报季度均衡性、严重报告表占比以及报告缺失项目等方面,进行对比分析实施监测技术应用前情况(2016年1月-2020年12月)和实施监测技术应用后情况(2023年1月-12月)。
3.2.1报告表上报季度均衡性及严重报告表占比明显上升
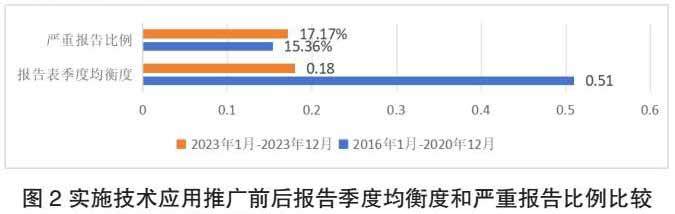
按季度计算报告表均衡度,计算方式为(∑|Xi-M|)/X,其中 Xi 为每季度报告表数,M 为四个季度的平均数,X 为报告表总数,即每季度报告表数量与全年季度报告表平均数之差的绝对值的总和,与报告表总数的比值,比值越小,均衡度越高。2016年1月-2020年12月1022份报告表上报季度均衡度为0.51,事件伤害程度为严重伤害的报告157份,占比15.36%;2023年1月-2023年12月1590份报告表上报季度均衡度为0.18,事件伤害程度为严重伤害的报告273份,占比17.17%。见图2。
3.2.2报告缺失项目明显减少
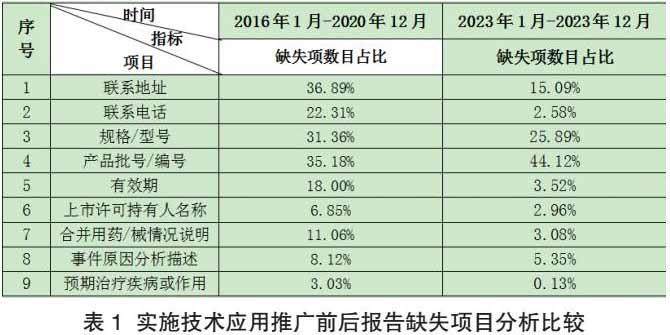
统计分析9项报告缺失率较高的项目,2023年1月-12月的缺失项数目占比较2016年1月-2020年12月的缺失项数目占比整体有所下降。见表1。
4.讨论与思考
4.1医疗器械不良事件上报情况
从2019年至2023年, 医疗器械不良事件上报数量整体呈增长趋势,2021年上报数量上升明显, 医疗机构上报意识和积极性得到了提高,但是上报的报告表全部都来自使用单位,医疗器械经营企业、持有人未履行报告义务,持有人主体责任未有效发挥。《医疗器械不良事件监测和再评价管理办法》明确了持有人、经营企业和使用单位为医疗器械不良事件报告上报法定主体,并突出了持有人应该持续开展药品上市后安全研究的责任和义务。从数据上看,持有人的实际工作与其应承担的主体责任存在较大差距。要改善此现状,必须从根本上提高持有人的认知,加强对持有人法规的学习贯彻,注重监测体系建设确保监测工作落实到位、不流于形式,强化培训,提升监测评价处置能力[5]。
4.2医疗器械不良事件报告表质量情况
从结果可知,实施监测技术应用后,报告表的季度均衡性和严重报告占比有了很大的提高,特别是季度均衡度,从0.51下降到0.18,均衡性明显提高,侧面也体现了整体报告表上报及时,迟报、漏报、补报的现象得到了改善。严重伤害的报告占比也从15.36%提升到17.17%,医护人员对加强严重伤害报告的收集上报意识有了一定的提高,但是根据医疗器械自身存在的固有风险、不良事件发生率、以及严重伤害报告表类型(可能导致严重伤害或者死亡的医疗器械不良事件。不良事件发生,虽然本次没有导致死亡或严重伤害,但是如果再次发生,或在患者危机情况下发生可能导致死亡或严重伤害;其他存在较大使用风险的。)可知,严重伤害的报告占比还有提升的空间。
从表1的报告项目缺失情况看,报告缺失数目占比整体有所下降,报告表完整性得到了改善。虽然整体的项目的缺失数量有所下降,但项目的缺失还有存在,还是会影响医疗器械不良事件潜在有价值信号的识别、提取,增加发现信号的难度。可进一步完善《医疗器械不良事件记录本》,增加缺失数量较多的项目;加大培训力度,减少因医疗机构监测人员频繁更换导致上报工作不熟悉情况;加强技术指导,在日常报告审核时及时跟上报单位沟通指导报告问题,切实提高报告质量。
4.3医疗器械风险管理情况
随着医疗机构上报意识逐渐增强、报告数量日渐增多,医疗器械风险、风险分析和风险管理已成为当前医疗器械研制、生产、经营、使用单位以及政府监管部门面对的重要而紧迫的课题[6]。以医疗器械风险管理为核心的监测工作重要性逐步凸显。通过开展风险管理工作,可以建立起使用单位反馈、持有人改进的正向循环,进一步完善医疗器械工艺,降低使用风险。目前,我市虽然在报告表数量、质量、风险控制意识方面有了提升,但是对于发现、研判风险信号的能力仍有待提高。为了保障医疗器械的安全性和有效性,及时发现和处理医疗器械不良事件,要加强医疗器械不良事件监测及风险预警[7]。积极探索医疗器械风险管理方法,不断完善监测技术手段,通过开展风险监测培训、风险案例研判会议,指导医院完善医疗器械临床使用安全监测和安全事件报告分析、评估、反馈机制,进一步提高监测人员从风险管理工作中不断积累经验和提升能力,做到快速、准确地从不良事件中发现问题和风险,及时控制风险,减少医疗器械不良事件的反复发生,保障公众生命安全和身体健康。
5.结论
综上所述,做好医疗器械不良事件报告的收集是开展上市后医疗器械风险管理的主要途径,提高报告质量保证每例报告的真实、完整、准确、及时是开展安全性监测与评价、数据有效利用的基础。通过设计规范记录本和工作手册、举办监测技术应用专场推广、开展质量评估会等方法,有效推动了使用单位积极上报医疗器械不良事件报告表,提高报告表质量,但是严重报告表占比还需进一步提高、持有人的实际工作与其应承担的主体责任存在较大差距,监测人员发现风险、评估风险能力还有待提高。需要不断完善监测措施、推广监测技术,通过加强技术支撑能力、开展有针对性的培训和宣传、创新报告和监测模式、加强数据共享、建立风险管理长效机制等方法,推动医疗器械风险发现、评估、防控,切实为人民群众用械安全筑牢坚实的屏障。
参考文献:
[1]董放,王刚,关薇,郑立佳.我国医疗器械不良事件信息管理机制研究[J].中国药物警戒 ,2016,13(3):148-153.
[2]国家市场监督管理总局. 医疗器械不良事件监测和再评价管理办法(国家市场监督管理总局、[2]国家卫生健康委员会令第1号)[EB/ OL].2021-6-24.https://www.samr.gov.cn/zw/zfxxgk/fdzdgknr/bgt/art/2023/art_4b69cde387db4c4fa4465aad987157e0.html.
[3]赵琦君,曾庆伟,谢宇越,曾玉珍.河源市基层医疗器械不良事件监测情况分析[J].中国医药科学,2024,14(8):134-138.
[4]张学宁,王玲,王刚,蔺旭东,杜红阳.医疗器械不良事件报告质量分析及改善对策[J].中国药物警戒,2015,(8):479-482,486.
[5]闫舒,刘莹.从持有人视角对医疗器械不良事件监测和再评价工作现状的调查与思考[J].医疗装备,2022,35(7):30-32.
[6]方涛.基层医疗器械不良事件监测及风险管理探讨[J].中国药物警戒,2009,6(5):302-304.
[7]李霞,杨锋,赵玉娟,于文雯,殷荐.医疗器械不良事件监测及风险控制管理方法[J].中国设备工程,2023,(15):198-200.
[8]刘慧萍.医疗器械不良事件风险管理思考[J].中国医疗器械信息,2017,23(23):133-135.
[9]史玉清.地市级监测机构医疗器械不良事件风险管理工作实践与探索[J].中国医疗器械信息,2023,29(17):7-10.
[10]翁飞,吴军,程时栋.”瑞士奶酪模型”在完善医疗器械不良事件监测管理中的应用[J].中国医院建筑与装备,2023,24(11):74-78.
[11]陈腾蛟.基层医疗器械不良事件监测工作存在的问题及建议[J].齐鲁药事,2012,31(2):121-122.
[12]陈凯,茅艳萍,李凯宇,王侃.医疗器械不良事件监测工作分析与管理[J].医疗装备,2022,35(8):6-11.
[13]王佳频,马相霞.医疗器械不良事件监测工作及管理研究[J].基层医学论坛,2022,26(23):93-95.






 京公网安备 11011302003690号
京公网安备 11011302003690号


