
- 收藏
- 加入书签
基于平均血小板体积分层指导的重症免疫性血小板减少症精准治疗策略:一项前瞻性多维度临床评价研究
摘要:
研究背景:重症免疫性血小板减少症(ITP)一线治疗(糖皮质激素/ 免疫球蛋白)无效率高达 30‰ 。平均血小板体积(MPV)可反映ITP 发病机制差异(血小板破坏或生成障碍),可能指导个体化治疗选择。
方法:前瞻性随机对照研究纳入2022 年1 月–2024 年11 月212 例血小板计数低于 30×10 ⁹ /L 的重症或其他需要紧急治疗的ITP 患者。随机分两组:常规组( n=106 ):随机选用地塞米松( 40mg/d×4d )静脉给药、免疫球蛋白( 1g.kg-1.d-1×2dΩ. )或重组人血小板生成素注射液( 300u/kg-1d-1×14d )。优化组( n=106 ):MPV>13fL 选抑制破坏药物地塞米松( 40mg/d×4d )静脉给药或免疫球蛋白( 1g.kg-1 . d-1×2d ), MPV⩽1 ⩽13fl 选择重组人血小板生成素注射液( 300u.kg-1 1. d-1×14d )。主要终点为治疗有效率;次要终点住院时间、费用和患者满意度。
结果:优化组有效率显著高于常规组( 86.8% vs. 71.7% , 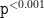 )。优化组起效时间大幅缩短(起效时间4.5 天 VS 7.0 天)。优化组住院天数(8.4 天 vs. 10.8 天)和费用(1.0 万元 vs. 1.53 万元)显著减少,患者满意度提升。
)。优化组起效时间大幅缩短(起效时间4.5 天 VS 7.0 天)。优化组住院天数(8.4 天 vs. 10.8 天)和费用(1.0 万元 vs. 1.53 万元)显著减少,患者满意度提升。
结论:MPV 分层治疗可精准匹配ITP 发病机制,显著提高疗效、缩短起效时间并降低医疗负担,尤其适用于基层医院。
关键词:平均血小板体积;重症免疫性血小板减少症;个体化治疗;疗效;医疗费用
研究背景
原发性免疫性血小板减少症(Primary immune thrombocytopenia, ITP)是一种以孤立性血小板减少为特征的出血性疾病,年发病率约 2-5/10 万,育龄女性及老年人高发 [1-3]。其发病机制复杂且异质性显著,核心是免疫失调: 60% 患者存在抗血小板糖蛋白(如 GPIIb/IIIa、GPIb/IX)自身抗体,介导脾巨噬细胞通过 FcγR 吞噬血小板,并激活 CD4 ⁺ T 细胞与 B 细胞相互作用,促进浆细胞产生抗体 [4-6] 。此外,非 FcγR 途径(如抗体介导血小板脱唾液酸化后被肝脏 ASGPR 清除)、ADAM10 金属蛋白酶介导的免疫调节、巨核细胞相关 miRNA 异常及感染(通过分子模拟或免疫激活)共同参与发病 [7-11]。当前一线治疗(糖皮质激素 / 免疫球蛋白)通过抑制抗体产生及血小板破坏起效,二线治疗(促血小板生成素受体激动剂TPO-RA 或免疫抑制剂)则促进血小板生成[3, 12]。然而,约 30% 患者对一线治疗无效,且缺乏早期预测疗效的指标,导致重症患者( PLT<10×10 ⁹ /L 或活动性出血)及需急诊手术者面临高风险 [13, 14]。基于血小板平均体积(Mean platelet volume, MPV)可反映 ITP 发病机制亚型(MPV 升高提示外周破坏为主,MPV 正常 / 轻度升高提示巨核细胞生成障碍)的特性 [15,16],及既往研究显示 MPV>13fl 对一线治疗有效性具 100% 特异性(AUC=0.69)[17],本研究拟评估MPV 指导分层治疗的临床价值。
病例与方法
1 病例:
本研究为前瞻性随机对照临床试验,旨在评估平均血小板体积(MPV)对重症原发性免疫性血小板减少症(ITP)患者治疗方案选择的指导价值。比较优化治疗组(基于 MPV 指导药物选择)与常规治疗组(随机选择指南推荐药物)的疗效和安全性,包括治疗有效率、起效时间、住院时间、费用及患者满意度等指标。研究于 2022 年 1 月至 2024 年 11 月在重庆市合川区人民医院进行,由该院血液内科负责执行。
1.1 入选标准:
纳入标准(受试者必须满足所有条件方可入组):
1.1.1 血小板计数低于 30×10 ⁹ /L 的重症或其他需要紧急治疗的原发免疫性血小板减少症(ITP)。具体定义为血小板计数低于 <10×10-9/L 且伴有活动性出血的患者;血小板<30×10⋅9/L 且出血评分 ⩾5 的患者;血小板 <30×10-9/L 且存在需紧急提升血小板数量的患者。
1.1.2 年龄 ⩾18 周岁。
1.1.3 能够充分理解研究要求,自愿签署知情同意书。
1.2 排除标准(符合任一条件即排除):
1.2.1 首次给药前12 周内接受过脾切除术。
1.2.2 已知对促血小板生成素或促血小板生成素受体激动剂无反应。
1.2.3 首次给药前2 周内接受过免疫球蛋白、糖皮质激素或其他免疫抑制剂治疗
1.2.4 首次给药前 4 周内接受过白介素 -11、促血小板生成素或促血小板生成素受体激动剂治疗。
1.2.5 首次给药前14 周内接受过抗体类药物(如利妥昔单抗)。
1.2.6 曾被诊断为抗磷脂抗体综合征或其他自身免疫性疾病(如系统性红斑狼疮)。
1.2.7 处于妊娠期、哺乳期或有妊娠计划。
1.2.8 有严重药物过敏反应史或已知对实验用药过敏
2 治疗方案:
2.1 符合纳入标准的患者随机分为两组,常规治疗组(对照组):随机选用地塞米松( 40mg/d×4d )静脉给药、免疫球蛋白 (1g.kg-1×2d )或重组人血小板生成素注射液( 300u kg-1.d-1×14d )中的任一给药方案。优化治疗组(试验组):基于 MPV 水平进一步细分:MPV>13fL 选抑制破坏药物地塞米松( 40mg/d×4d )静脉给药或免疫球蛋白( 1g.kg-1×2d ),MPV⩽13fL 选择重组人血小板生成素注射液 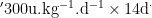 )。
)。
2.2 具体治疗措施:所有患者治疗后每 3 天复查一次血常规,监测血小板计数和 MPV。血常规检测使用 EDTA 抗凝标本,通过全自动血细胞分析仪(型号:CAL8000)进行。治疗药物包括:地塞米松,静脉用免疫球蛋白,重组人血小板生成素注射液。
2.3 治疗流程:诊断依据《成人原发免疫性血小板减少症诊断与治疗中国指南(2020 年版)》。随机分组后,根据 MPV 结果指导优化组药物选择,常规组随机用药。治疗后评估指标包括有效(定义为治疗至血小板计数≥ 30×10-9/L ,比基础血小板计数增加至少 2 倍,且无出血表现),起效时间(定义为治疗至达有效标准的时间)、住院时间、费用和患者满意度。
3 疗效评价:主要终点为治疗有效率(治疗有效定义为治疗至血小板计数 ⩾30×10∘9/L ,比基础血小板计数增加至少 2 倍,且无出血表现)。次要终点为起效时间:定义为治疗至达有效标准的时间。住院总时间,治疗费用,患者满意度。
评价方法为通过定期血常规检测(每 3 天一次)记录血小板变化,并结合临床指标(如出血症状改善)进行评估。
4 随访:研究期间(2022 年 1 月至 2024 年 11 月)收集病例数据,后续在 2024 年 12 月至 2025 年 1 月进行数据整理和统计分析。主要追踪治疗反应、不良反应事件及起效时间、住院时间。
5 统计学方法:应用 R 4.4.2 版本软件进行统计学分析。计量资料的组间比较采用 t 检验,当组间计量资料不符合正态分布或组间计量资料方差不齐时采用 Mann-Whitney U 秩和检验,分类变量的组间比较采用 χ2 检验,当不满足 χ2 检验时应用 Fisher 检验, P<0.05 为差异
有统计学意义。
基金项目:合川区科技计划项目(HYKYLL-2021-19)
利益冲突:所有作者声明不存在利益冲突
作者贡献声明:邱秋:完成论文设计,采集数据,分析、解释数据,起草文章;李国均:课题指导和修稿。
结果
1 患者临床特征:本研究最终有 206 例患者符合试验入排标准,其中常规组 106 例,优化组 106 例。常规组患者的平均年龄为 54.2 岁,优化组患者的平均年龄为 56.8 岁。入组时疾病状态:血小板计数低于 <10×10-9/L 且伴有活动性出血的患者有 83 例,血小板<30×10-9/L 且出血评分 ⩾5 的患者有 72 例,血小板 <30×10-9/L 且存在需紧急提升血小板数量情况的患者有 57 例。按照血小板体积进行分组后,平均血小板体积 >13 fl 的患者在常规组和优化组分别为 25 和 27 例,平均血小板体积 ⩽ 13 fl 的患者在常规组和优化组分别为81 和79 例,两组患者的临床特征差异无统计学意义(Table 1)。但是在分析常规组和优化组之间的治疗方案相关病例数时,发现两组之间存在统计学差异, p<0.001 (Table 1)。
2 患者疗效和治疗性价比分析:首先我们分析患者的治疗有效率,与常规组相比( 71.7% ),优化组的治疗有效率达到 86.8% ,效果显著(Figure 1a)。同时,分析治疗起效时间时也发现,优化组的平均起效时间缩短到 4.5 天,而常规组为 7 天(Figure 1b)。除了疗效之外,分析患者的住院时间,住院费用和满意度时发现也有显著改善。比如优化组与常规组相比,患者的平均住院时间从 10.8 天缩短到 8.4 天(Figure 2a, Table 2),患者的平均住院费用从 1.53 万减少为 1 万(Figure 2b, Table 2),患者的住院满意度也得到大幅提升(Figure 2c,Table 2)。以上数据提示我们,基于 MPV 进行的分层治疗方案有效的改善了重度免疫原性血小板减少症患者的身体状态和治疗性价比。
讨论
本研究首次证实 MPV 分层治疗策略对重症 ITP 的显著优化价值。优化组(基于 MPV 指导药物选择)治疗有效率高达 86.8% (常规组 71.7% , p<0.001 ),起效时间缩短 35.7% (4.5天 vs 7.0 天)。这一结果直接解决约 30% 患者对一线治疗无效的临床困境,为快速提升血小板、降低出血风险提供实证支持。
MPV>13fl(提示血小板破坏为主)患者接受糖皮质激素 / 免疫球蛋白治疗有效率达89.3% , MPV⩽13fl (提示生成障碍为主)患者采用促生成药物(rhTPO)有效率达 84.8% 。该策略精准匹配 ITP 异质性发病机制(如抗体介导破坏 vs 巨核细胞凋亡),同时显著降低医疗负担:住院时间缩短 22.2% (8.4 天 vs 10.8 天),费用减少 34.6% (1.0 万元 vs 1.53 万元),患者高满意度比例提升3 倍以上( 57% vs 18% ),避免无效治疗经济负担。
尽管本研究取得可喜的结果,但是当前研究仍然存在三方面局限:1 单中心样本偏差:仅纳入合川区病例,未覆盖多地域人群;2 机制深度不足:未联合骨髓巨核细胞增生情况、血小板相关抗体、ADAM10、miRNA 等关键标志物深化分层机制;3 长期数据缺失:缺乏复发率及 rhTPO 安全性追踪(如血液升高、关节疼痛等)。未来仍需开展多中心验证(尤其基层医院),结合基因组技术开发 "MPV+ 免疫标志物" 复合模型,并补充卫生经济学评估。
总之,MPV 分层策略将ITP 治疗推向精准化、高效化、普惠化新阶段。其核心优势在于基层普适性(MPV 检测成本低廉、技术普及),急诊价值(为 PLT<10×10 ⁹ /L 伴出血或急诊手术患者赢得关键时间窗),和指南革新潜力(研究结果有望推动国际指南纳入 MPV 作为治疗分层指标)。未来,需要通过产学研协作,开发床旁快速检测设备并拓展至儿童ITP 人群,最终实现个体化治疗的全面落地。
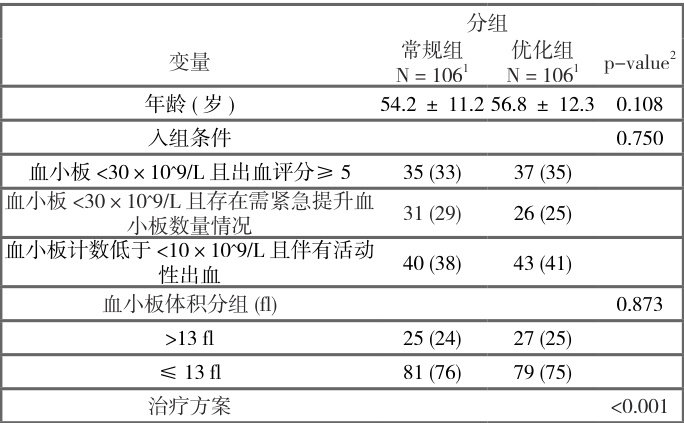
Tables and Figure legends Table 1. 临床患者基线特征

Table 2. 患者治疗效果比较

Figure legend
Figure 1 免疫性血小板减少症患者治疗有效率和起效时间分析
常规组和优化组之间免疫性血小板减少症患者治疗有效率分析;(b)常规组和优化组之间免疫性血小板减少症患者治疗起效时间分析;
Figure 1

Figure 2 免疫性血小板减少症患者相关经济价值分析
常规组和优化组之间的免疫性血小板减少症患者治疗后住院时间分析;(b) 常规组和优化组之间的免疫性血小板减少症患者住院费用分析;(c) 常规组和优化组之间的免疫性血小板减少症患者住院满意度分析;
Figure 2

参考文献:
1. Puneet Kaur Sahi, Chandra J. Immune Thrombocytopenia_ American Society of Hematology Guidelines. Indian Pediatr 2020, 57(9): 854-856. 2. Kohli R, Chaturvedi S. Epidemiology and Clinical Manifestations of Immune Thrombocytopenia. Hämostaseologie 2019, 39(03): 238-249. 3. Thrombosis and Hemostasis Group CSoH, Chinese Medical Association. Chinese guideline on the diagnosis and management of adult primary immune thrombocytopenia (version 2020). Zhonghua Xue Ye Xue Za Zhi 2020, 41(8): 617-623. 4. Audia S, Mahévas M, Samson M, et al. Pathogenesis of immune thrombocytopenia. Autoimmunity Reviews 2017, 16(6): 620-632. 5. Marini I, Bakchoul T. Pathophysiology of Autoimmune Thrombocytopenia: Current Insight with a Focus on Thrombopoiesis. Hämostaseologie 2019, 39(03): 227-237. 6. Wang Q, Li J, Yu T-s, et al. Disrupted balance of CD4+ T-cell subsets in bone marrow of patients with primary immune thrombocytopenia. International Journal of Biological Sciences 2019, 15(13): 2798-2814. 7. Grozovsky R, Begonja AJ, Liu K, et al. The Ashwell-Morell receptor regulates hepatic thrombopoietin production via JAK2-STAT3 signaling. Nature Medicine 2014, 21(1): 47- 54. 8. Lambert MP, Gernsheimer TB. Clinical updates in adult immune thrombocytopenia. Blood 2017, 129(21): 2829-2835. 9. Lownik JC, Luker AJ, Damle SR, et al. ADAM10-Mediated ICOS Ligand Shedding on B Cells Is Necessary for Proper T Cell ICOS Regulation and T Follicular Helper Responses. The Journal of Immunology 2017, 199(7): 2305-2315. 10. Deng G, Yu S, He Y, et al. MicroRNA profiling of platelets from immune thrombocytopenia and target gene prediction. Molecular Medicine Reports 2017, 16(3): 2835-2843. 11. Kuwana M. Helicobacter pylori-associated immune thrombocytopenia: Clinical features and pathogenic mechanisms. World Journal of Gastroenterology 2014, 20(3). 12. Provan D, Arnold DM, Bussel JB, et al. Updated international consensus report on the investigation and management of primary immune thrombocytopenia. Blood Advances 2019, 3(22): 3780-3817. 13. Jouzdani S, Sadeghi A, Hosseini S. Evaluation of treatment plan by three-period pulses of high-dose dexamethasone among patients with primary immune thrombocytopenia on platelet count response and adverse events: A randomized Clinical trial. Journal of Research in Medical Sciences 2020, 25(1). 14. Yu Y, Wang M, Hou Y, et al. High‐dose dexamethasone plus recombinant human thrombopoietin vs high‐dose dexamethasone alone as frontline treatment for newly diagnosed adult primary immune thrombocytopenia: A prospective, multicenter, randomized trial. American Journal of Hematology 2020, 95(12): 1542-1552. 15. Norrasethada L, Khumpoo W, Rattarittamrong E, et al. The Use of Mean Platelet Volume for Distinguishing the Causes of Thrombocytopenia in Adult Patients. Hematology Reports 2019, 11(1). 16. Stefan Handtke, Thiele T. Large and small platelets-(When) do they differ? J Thromb Haemost 2020, 18(6): 1256-1267. 17. AkkuŞ E, FİDan Ç, DemİRcİ G, et al. Mean platelet volume and response to the first line therapy in newly diagnosed adult immune thrombocytopenia patients: a retrospective study. Turkish Journal of Medical Sciences 2020, 50(4): 798-803.
基金项目:合川区科技计划项目(HYKYLL-2021-19)
利益冲突:所有作者声明不存在利益冲突
作者贡献声明:邱秋:完成论文设计,采集数据,分析、解释数据,起草文章;李国均:课题指导和修稿。
课题项目名称:基于平均血小板体积指导重症原发免疫性血小板减少症治疗方案选择的研究
项目编号:HYKYLL-2021-19课题主管部门:重庆市合川区科学技术局
作者简介:
姓名:邱秋,性别:女,出生年月:1987、09、,民族:汉族,籍贯:重庆市合川区,最高学历:博士,职称:副主任医师,单位:重庆市合川区人民医院,科室:消化内科,主要研究方向:消化道出血 消化系统恶性肿瘤。
姓名:李国均,性别:男,出生年月:1982、03,民族:汉族,籍贯:四川广安,最高学历:硕士,职称:副主任医师,单位:重庆市合川区人民医院,科室:血液内科,主要研究方向:血液肿瘤及出凝血疾病。






 京公网安备 11011302003690号
京公网安备 11011302003690号


